摘要:
在生物基呋喃类缓蚀剂的研究基础上,利用Tafel极化曲线和电化学阻抗技术 (EIS) 研究了Q235碳钢在不同浓度的糠醇缩水甘油醚 (FGE) 盐酸溶液中的腐蚀行为,并通过静态失重实验分析了Q235碳钢在不同体系中的腐蚀速率。结果表明,4.92×10-4 molL-1的FGE对Q235碳钢具有最好的缓蚀效果,其缓蚀效率达到94.0%,腐蚀速率为0.076 mgcm-2h-1。此外,经证明FGE在Q235碳钢表面的吸附过程符合Langmuir吸附模型,同时发生物理吸附和化学吸附。
关键词: 生物基 ; 呋喃类缓蚀剂 ; FGE ; Q235碳钢 ; Langmuir吸附模型
碳钢无论是在工业或是农业领域都得到了广泛的应用。然而,碳钢本身具有的严重腐蚀倾向使其在酸性介质中的应用受到了极大限制。如石油工业中的酸化过程采用15%的盐酸溶液进行,其存储酸液的设备由Q235或N80碳钢制得,这些设备在高浓酸条件下极易造成腐蚀破坏。在酸性介质中添加缓蚀剂是减缓或阻止碳钢腐蚀的最有效方法之一[1,2,3,4,5,6,7]。目前,工业上常用的缓蚀剂主要是一类含有N,S和O等原子、结构中含有重键或分子量较大的有机化合物,其公认的缓蚀机理是与金属表面的吸附作用。尽管有机缓蚀剂具有令人满意的缓蚀效果,但它却具有较强的毒性和皮肤刺激性,这对人体和环境都造成了一定的威胁。近些年来,随着人们环保意识的不断增强和可持续发展思想的逐渐深入,对缓蚀剂的开发和应用也提出了越来越多的新要求。围绕高性能、低成本、可再生等目标,绿色化学的思想研究和制备环境友好型的生物基缓蚀剂,逐渐成为新世纪缓蚀剂发展的重点方向[8,9,10,11,12,13]。
糠醇缩水甘油醚 (FGE) 可从糠醇和环氧氯丙烷合成得到,而糠醇可从生物质得到,环氧氯丙烷可从生物基甘油得到,因此FGE是一种生物基材料,并且在自修复涂料、半导体材料中有广泛应用[14,15,16,17]。FGE带有一个呋喃环和一个环氧基团,而文献[11,18,19]指出呋喃环具有缓蚀作用。Vishwanatham等[11]将糠醇作为在15% (质量分数) 盐酸条件下N80钢的缓蚀剂,结果表明糠醇的缓蚀率与浓度几乎成线性关系,当浓度为80 mmol/L时,缓蚀效率高达91%。France[18]指出在酸性介质中呋喃及其衍生物是以质子化形式起缓蚀作用的。颜肖慈等[19]证明了呋喃及其邻位取代物:—CH3,—I,—CHO,—COOH和—NO2在盐酸介质中对Al的腐蚀起到一定的缓蚀作用,并利用AM1量子化学计算方法建立了Al族界面模型,结果表明呋喃及其衍生物是以形成配合物来减缓Al的腐蚀。因此可以推断,FGE具有良好的缓蚀效果。此外,FGE的环氧基团是极性基团,可以预见环氧基团将提高FGE的成膜性,从而提高其缓蚀性能。但是截至目前,未见有关于FGE缓蚀性能的报道。基于此,本文使用电化学方法、静态失重实验和扫描电镜 (SEM) 等表征手段研究了FGE对Q235碳钢在0.5 mol/L HCl溶液中的缓蚀行为及缓蚀机理,以期为FGE作为一种绿色缓蚀剂的应用提供理论基础。
1 实验方法
1.1 碳钢电极的制备及电化学测试
Q235碳钢由山东晟鑫科技公司提供,碳钢电极使用环氧树脂密封制成,电极裸露表面积为1 mm×1 mm。先用水磨砂纸 (60~2000#) 逐级打磨抛光后,用丙酮冲洗表面,冷风吹干后置于0.5 mol/L的含不同浓度FGE缓蚀剂 (0,1.64×10-4,3.28×10-4,4.92×10-4和6.56×10-4 mol/L) 的盐酸溶液中,浸泡3 h后进行耐蚀性能测试。FGE根据先前的工作由实验室自制[20](VEP=0.55 eq/100 g,室温下黏度26 mPa·s)。测量采用经典三电极体系,碳钢电极为工作电极,Pt电极为辅助电极,参比电极为饱和甘汞电极。分别测试碳钢在不同浓度缓蚀剂溶液中的电化学阻抗谱 (EIS) 及动电位极化曲线,每组测试含3个平行试样。电化学测试采用CHI660E电化学工作站,扫描速率为0.5 mV/s,扫描范围为-200~200 mV (相对于OCP),以CHI660E自带Specialanalysis软件在Tafel区拟合。
1.2 静态失重实验
静态失重实验参照GB10124-88执行,将经200~1200#砂纸打磨光滑的Q235碳钢试样 (10 mm×10 mm×10 mm) 室温下浸泡于含不同浓度FGE的0.5 mol/L的HCl溶液中,3 h后取出经去离子水和无水乙醇清洗,吹干后对其质量变化进行记录和分析并计算出腐蚀速率V、FGE在Q235碳钢表面的覆盖率θ和缓蚀效率CR[21]。

其中,ΔW代表Q235碳钢在盐酸溶液中的失重,s表示Q235碳钢试样表面积,t代表浸泡时间,V0与V分别表示Q235碳钢在空白溶液和加入缓蚀剂FGE的HCl溶液中的腐蚀速率。
1.3 碳钢电极表面形貌
将经不同盐酸溶液浸泡后的Q235碳钢在SEM(FEI Quanta FEG 250) 下观察其表面形貌变化。
2 结果与讨论
2.1 缓蚀剂的电化学性能
图2和表1分别是Q235碳钢在含不同浓度FGE的0.5 mol/L盐酸溶液中浸泡3 h的动电位极化曲线 (Tafel曲线) 和使用CHI660E自带Specialanalysis软件拟合获得的电化学参数。可以看出,加入不同浓度的FGE后,自腐蚀电位发生偏移,相较于不添加FGE Q235碳钢的Tafel曲线,含有1.64×10-4 mg/L FGE Q235碳钢的自腐蚀电位正移,而含有其他3种浓度FGE的溶液中Q235碳钢的自腐蚀电位负移。此外,βa与βc均发生了变化,这说明电极的阳极和阴极反应均受到缓蚀剂FGE的影响,即FGE是一种混合型缓蚀剂。通常,Tafel曲线的极化电流密度Icorr可用来表征缓蚀剂对Q235碳钢的保护效果[22]。一般地,Icorr值越大,缓蚀剂的缓蚀性能越差;Icorr值越小,其缓蚀效果就越好。从图2和表1可以看出,FGE的Tafel曲线的Icorr值随着缓蚀剂浓度的增加呈现先减小后增加的趋势,且当FGE浓度为4.92×10-4 mol·L-1时,所对应的Icorr值达到最小,为11.74 ?A·cm-2。
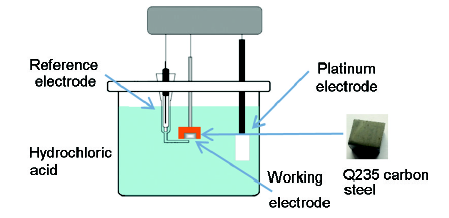
图1 电化学工作站三电极实验系统
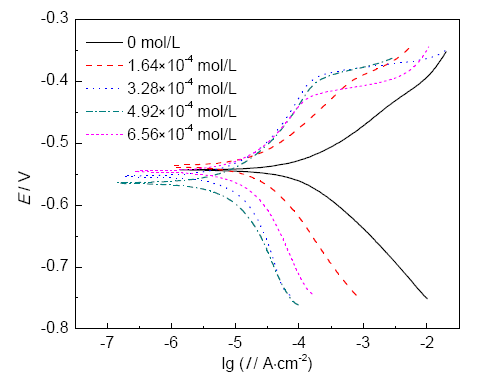
图2 Q235碳钢在含不同浓度FGE缓蚀剂的0.5 mol/L盐酸溶液中浸泡3 h的极化曲线
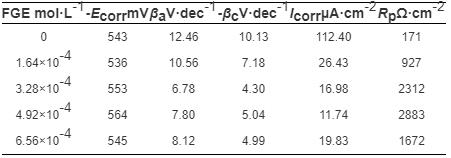
表1极化曲线拟合后的电化学参数
为了进一步分析室温下FGE在Q235碳钢表面的吸附类型和缓蚀效果,分别测定了Q235碳钢在空白盐酸电解液和加有缓蚀剂FGE电解液的EIS,结果见图3。一般,在EIS曲线中高频区域容抗弧是由溶液中电荷转移引起的,且容抗弧半径越大证明缓蚀效果越好。从图3a可以看出,在含FGE电解液中高频区容抗弧的半径远远大于在空白溶液中的,说明电解液中加入FGE后,溶液中电荷转移的阻力大幅度增加,Q235碳钢的腐蚀速率减小。由此可以得出,FGE对Q235碳钢起到了很好的缓蚀效果。
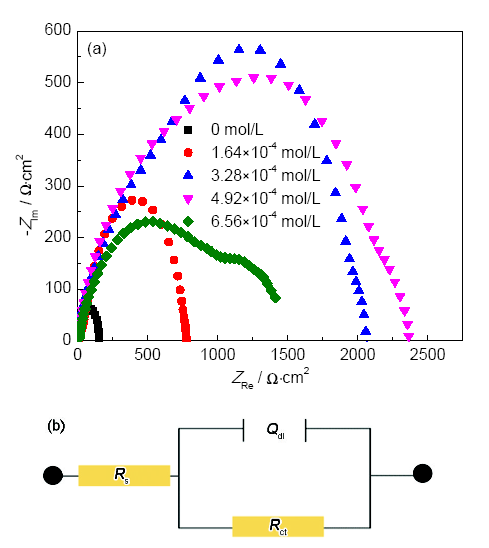
图3 Q235碳钢在含不同浓度FGE的0.5 mol/L盐酸溶液中浸泡3 h的电化学阻抗谱和等效电路图
为了定量研究缓蚀剂对Q235碳钢的防护效果,采用ZSimpWin3.21软件中的等效电路R(QR) (图3b) 进行拟合。其中,Rs为溶液电阻;n为常相位角指数,表征弥散效应程度;Qdl为腐蚀介质与金属之间的双电层电容,用来反映FGE在电极表面的吸附特性;Rct为溶液的电荷转移电阻,表征碳钢腐蚀速率,其值越大,表面腐蚀越缓慢。所得到的电化学参数拟合结果见表2。
表2 EIS拟合后的电化学参数
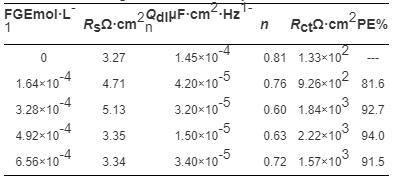
由表2可知,与空白溶液相比,添加FGE后盐酸溶液体系的Rs值几乎未发生变化;溶液的Qdl值随着FGE浓度的增加呈现先减小后增加的趋势。其原因为,盐酸体系中的FGE可以在碳钢表面形成吸附层,取代了吸附于金属表面的介电常数较大的水分子,而当FGE浓度达到一定值时出现了脱附现象。另外,空白盐酸溶液的Rct值为133.60 Ω·cm2,当体系中FGE浓度逐渐增加时,溶液的Rct值出现了先增加后减小的趋势;当FGE的浓度由1.64×10-4 mol·L-1逐渐增加到6.56×10-4 mol·L-1时,Rct先从925.5 Ω·cm2逐渐增加到2217.0 Ω·cm2,然后又降至1517.0 Ω·cm2,其Rct始终远远大于空白体系的。另外,溶液的缓蚀效率可以根据下式得出,结果见表2。
![]()
其中,R0ct和Rct分别为空白体系和加入缓蚀剂后溶液的电荷转移电阻。由表2可知,当盐酸体系中FGE的浓度为4.92×10-4 mol·L-1时,其缓蚀效率达到最大值94.0%。由此得出,FGE对碳钢在盐酸中的腐蚀具有较好的抑止作用,且浓度为4.92×10-4 mol·L-1的FGE对碳钢的缓蚀效率最佳,该结果与Tafel极化曲线结果相一致。
2.2 静态失重实验
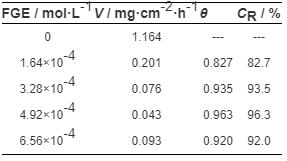
静态失重结果如表3所示。可知,添加0,1.64×10-4,3.28×10-4,4.92×10-4和6.56×10-4 mol/L FGE的盐酸体系中,碳钢的腐蚀速率分别为1.164,0.201,0.076,0.043和0.093 mg·cm-2·h-1,其缓蚀效率分别为82.7%,93.5%,96.3%和92.0%。该结果进一步证明FGE的加入可以显著降低碳钢在酸性溶液中的腐蚀速率,且其浓度为4.92×10-4 mol·L-1时对碳钢具有最佳的缓蚀作用。
表3 Q235碳钢在含不同浓度FGE的0.5 mol/L盐酸溶液中的失重实验结果
2.3表面分析
图4为室温下碳钢电极在含不同浓度FGE的0.5 mol/L盐酸体系中浸泡3 h后表面的SEM像。可以看出,在不含缓蚀剂FGE的盐酸体系中,碳钢表面出现大量的黄色腐蚀产物和严重的裂痕,而在含有4.92×10-4 mol/L FGE的盐酸溶液中浸泡后的碳钢表面没有观察到明显的腐蚀或裂纹产生,说明FGE能够很好地抑制碳钢的腐蚀,对其具有良好的缓蚀作用。
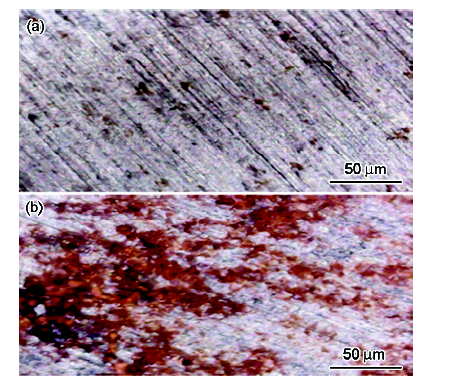
图4 Q235碳钢在含4.92×10-4 mol/L的FGE和空白盐酸溶液中浸泡3 h后的SEM像
2.4 吸附等温线和吸附机理
缓蚀剂吸附能力通常用来表征其缓蚀效率的高低,利用吸附等温线判断缓蚀剂与金属表面的作用类型和大小。缓蚀剂在碳钢表面的覆盖率θ见表3。可以看出,碳钢表面缓蚀剂的覆盖率随着FGE浓度的增加先增加后减小,当浓度为4.92×10-4 mol·L-1时覆盖度达到最大值0.963;而继续增大FGE浓度时,覆盖率出现了减小的趋势,说明此时FGE出现了脱附的现象。
缓蚀剂常用的吸附模型主要分为3种:Temkin吸附模型、Freundlich吸附模型和Langmuir吸附模型。根据文献[23],Langmuir吸附模型较为符合缓蚀剂的吸附机理。本实验假设FGE的吸附为Langmuir吸附模型,吸附方程为:
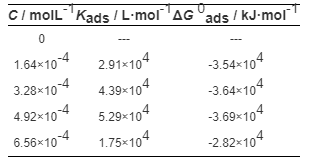
表4 FGE在碳钢表面的吸附参数
![]()
其中,C为缓蚀剂的浓度 (mol·L-1),Kads是吸附平衡常数 (L·mol-1)。FGE的吸附自由能△G 0ads由下式得到:
![]()
其中,R为气体平衡常数8.314 J/ (mol·K),T为温度(K),55为水的浓度 (mol·L-1)。Kads和△G0ads的计算结果列于表4中。
对室温下 (298 K) 的C/θ与C进行线性处理,由图5a可知,FGE的C/θ与C较好的符合线性关系,属于Langmuir吸附模型。文献[20]指出,当活化能△G0ads的值在0~-20 kJ·mol-1之间时,其吸附类型属于静电物理吸附;当活化能△G0ads的值小于-40 kJ·mol-1时,其吸附属于化学吸附,是由缓蚀剂分子和金属表面之间形成强烈的共价键造成的。本实验中,FGE的活化能△G0ads值介于-28~-36 kJ·mol-1之间,说明缓蚀剂FGE和Q235碳钢之间为物理吸附和化学吸附同时存在的混合型吸附,即FGE对金属的吸附既有静电作用的物理吸附,又具有共价键作用的化学吸附。
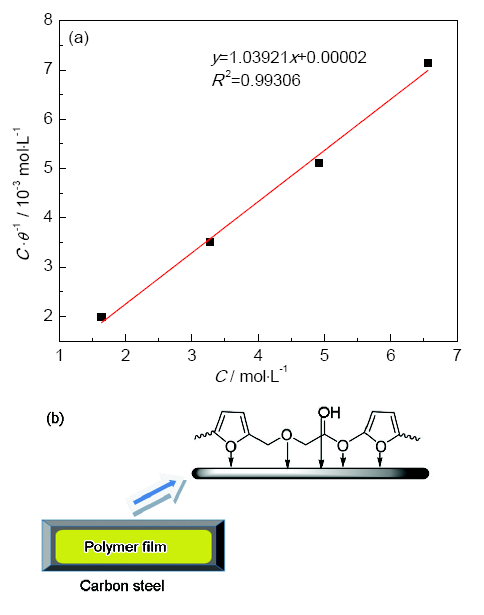
图5 FGE的Langmuir吸附等温线和FGE在碳钢表面的吸附机理示意图
图5b为FGE在碳钢表面可能的吸附机理。FGE在盐酸溶液中发生环氧基团的开环反应和呋喃环的聚合反应。聚合物中具有大量的含孤对电子的O原子,可与金属空d轨道形成化学配位键,产生大量金属螯合物并吸附于金属表面。另外,聚合物大分子能够形成空间网络屏障结构覆盖于金属表面,阻碍水分子和Cl-的进攻,起到了较好的物理屏蔽作用。随着FGE浓度的增加,覆盖膜也随之增加,缓蚀效率逐渐提升。而当缓蚀剂增加到一定浓度时,缓蚀效率出现下降且溶液由浑浊变为澄清并有少许沉淀产生,其原因在于溶液中金属螯合物的浓度大于其溶度积,促使聚合物出现脱附现象,从而导致缓蚀剂的缓蚀效率下降。
3 结论
(1) 通过Tafel极化曲线分析了呋喃类缓蚀剂FGE对Q235碳钢在0.5 mol/L HCl中的缓蚀效果,证明FGE具有较佳的缓蚀性能,其中含4.92×10-4 mol·L-1的FGE对金属的缓蚀效率最高达到94.0%。
(2) Langmuir吸附等温线证明FGE在碳钢表面属于物理和化学混合型吸附;FGE在盐酸溶液中发生聚合,并在金属表面形成螯合物覆盖膜,减缓了金属的腐蚀速率。
The authors have declared that no competing interests exist.
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。
-
标签: 生物基, 呋喃类缓蚀剂, FGE, Q235碳钢, Langmuir吸附模型

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





