热烈庆祝
上海材料研究所有限公司
值此欢庆之时,分析一篇上海材料研究所有限公司的科研文章《环境因素对地铁钢轨用U75V钢腐蚀行为的影响》。
环境因素对地铁钢轨用U75V钢腐蚀行为的影响
何兆如,纪开强,李光福
(上海材料研究所有限公司 上海市工程材料应用与评价重点实验室)
地铁钢轨在潮湿甚至积水的隧道环境中会出现明显的腐蚀,钢轨的锈蚀将导致经济损失甚至威胁到地铁的安全可靠运行。国内外针对钢轨的腐蚀问题已进行了相关研究,包括环境因素、显微组织、加工工艺等对钢轨腐蚀的影响。其中,环境因素导致钢轨腐蚀失效的问题值得关注。
上海地铁主要使用U75V钢制造的钢轨,关于U75V钢的腐蚀问题,已有学者做了一些研究,主要包括U75V钢的早期腐蚀行为及其在模拟环境中的缝隙腐蚀行为,但是针对该钢在地铁隧道环境中的腐蚀研究还不够深入。因此,深入研究其影响因素、重要规律和机理,探索防护方法有重要意义。
本工作以上海市地铁隧道某地段的U75V钢轨失效件为研究对象,通过浸泡试验和腐蚀电化学试验研究其腐蚀行为及溶液浓度和温度的影响,并采用溶液除氧的方式探索其腐蚀机理,以期为寻找钢轨的腐蚀防护方法提供理论基础。
01 试验材料与方法
试验材料
试验材料取自上海地铁某隧道环境中服役一段时间后因腐蚀失效而更换下来的钢轨底部。该钢轨为U75V型,其显微组织为典型的片层状珠光体组织。
浸泡试验
根据JB/T 7901-2001《金属材料实验室均匀腐蚀全浸试验方法》进行浸泡试验,采用线切割从失效钢轨底部位置取样,尺寸为50 mm×25 mm×5 mm。用氧化铝砂纸逐级打磨试样后,采用1 μm金刚石抛光液抛光,清洗干燥后测量试样尺寸并称量。
在敞口于空气的不同质量分数(1.0%、3.0%、5.0%、10.0%)NaCl溶液中,每种浓度条件下设三片试样,30 ℃恒温浸泡90天,每30天取出一片试样,清洗并用毛刷去除腐蚀产物、干燥、称量,计算腐蚀速率。试验结果取三片试样的平均值。
电化学试验
参照TCSCP0035.15-2017《低合金结构钢试验室腐蚀试验 第15部分:低合金结构钢腐蚀电化学试验方法》进行腐蚀电化学试验,用ZF-100电化学工作站测试动电位极化曲线,通过Tafel外推法计算自腐蚀电流密度,并通过Faraday定律换算得到腐蚀速率。
测试主要是在敞口烧杯中进行,采用三电极体系,辅助电极为铂电极,参比电极为饱和甘汞电极(SCE),工作电极为试样。相对自腐蚀电位-0.20 V开始动电位极化曲线扫描,扫描速率0.5 mV/s。试验溶液为不同质量分数(1.0%、2.0%、3.0%、3.5%、5.0%、10.0%)NaCl溶液,温度为10,30,50 ℃。
另进行除氧试验以对比研究溶液中氧的影响,探索腐蚀机理。具体操作为:采用五口瓶,在测试前向溶液中通入纯度为99.999%氮气预除氧30分钟,并在整个试验过程中持续通入氮气除氧。用光学显微镜和扫描电镜观察试样。
02 试验结果与讨论
浸泡试验
由图1可见:在30 ℃的1.0% NaCl溶液中浸泡90天后,试样宏观上表现为均匀腐蚀,微观上可以直接观察到腐蚀后产生的片层状珠光体。
(a)OM形貌
(b)SEM形貌
图1 试样在30 ℃的1.0% NaCl溶液中浸泡90天后的腐蚀形貌
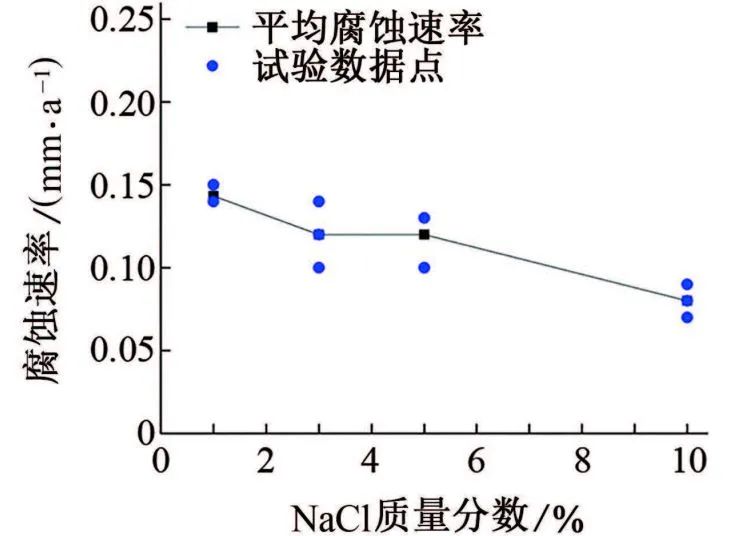
由图2可见:随着NaCl浓度的升高,试样的腐蚀速率呈现缓慢下降的趋势,但并不显著。
图2 试样在30 ℃、不同浓度NaCl溶液中的腐蚀速率
电化学试验
NaCl浓度的影响
由图3可见:试样的腐蚀速率随着NaCl浓度升高呈现下降的趋势,这与浸泡试验结果相似,但腐蚀速率低于浸泡试验结果。
(a)自腐蚀电位(Ecorr)30 ℃
(b)自腐蚀电流密度(Jcorr)30 ℃
(c)腐蚀速率(vcorr)30 ℃
图3 试样在不同浓度NaCl溶液中的电化学试验结果
这可能是因为浸泡试验时间相对较长,表面被大量腐蚀产物包覆而受到某种保护,所以腐蚀速率较低。当NaCl质量分数较低时,试验结果有一定离散性,但随着NaCl质量分数的升高,离散性减小。NaCl质量分数对腐蚀行为的影响机理还有待研究。
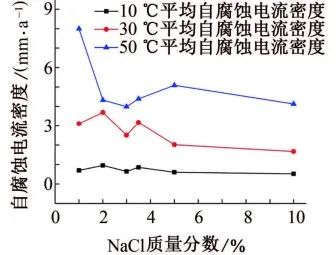
温度的影响
由图3还可见:随着温度的升高,试样的平均自腐蚀电流密度明显升高,即腐蚀速率升高。试样的阳极和阴极过程反应式如下:
阳极过程:
Fe→Fe2++2e- 或 Fe3++3e- (1)
阴极过程:
O2+2H2O+4e-→4OH-
氧去极化反应式 (溶液中氧较充分时) (2)
2H2O+2e-→H2+2OH-
或 2H++2e-→H2
氢去极化反应式 (溶液中缺氧时) (3)
可以认为在阳极过程方面,温度升高加速电极反应,导致腐蚀速率随着温度的升高而加快;阴极过程方面,温度升高使水中物质的扩散系数增大,更多的溶解氧扩散到金属表面的阴极区,加速腐蚀。
溶解氧的影响
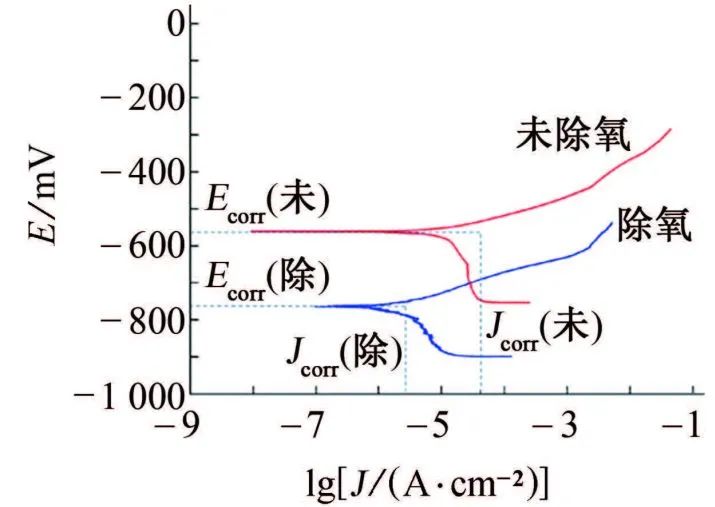
由图4和图5可见:试样在未除氧环境中的腐蚀电流密度和自腐蚀电位显著高于除氧环境中的。
(a)1.0% NaCl
(b)10.0% NaCl
图4 试样在30 ℃除氧与未除氧试验溶液中的极化曲线
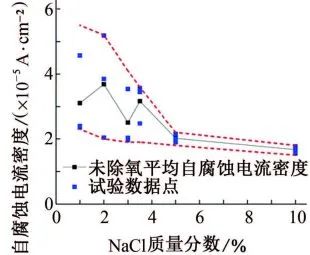
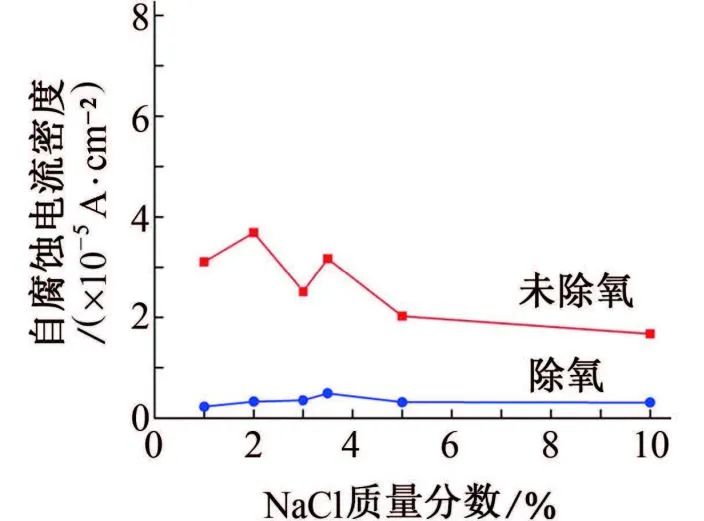
图5 试样在30 ℃除氧与未除氧的不同NaCl质量分数试验溶液中的平均自腐蚀电流密度
这是因为未除氧时,由于溶液中富氧,阴极极化为氧去极化过程;随着溶液中氧含量降低,阴极过程变成氧去极化-氢去极化综合控制;充分除氧后,阴极极化过程变成氢去极化主导,因此自腐蚀电位和腐蚀速率显著下降。即在含有氧气的环境中,试样更容易发生腐蚀。
由图4还可见:试样在未除氧与除氧环境中的极化曲线均无明显的过钝化材料应有的阳极反应特征,属于活化极化控制的腐蚀体系。该体系主要是受阴极控制的腐蚀过程,而溶液中的氧含量会影响阴极的腐蚀过程。在氧气充分的情况下,自腐蚀电位、自腐蚀电流密度均大于除氧情况下,腐蚀速率也明显较高。而在除氧溶液中,NaCl浓度对试样腐蚀速率的影响很小。
03 结论
(1) 在敞开于空气中的NaCl溶液中,钢轨试样的腐蚀速率随着NaCl含量的升高而下降。
(2) 在本试验温度范围内(10~50 ℃),钢轨试样的腐蚀速率随着温度的升高而升高。
(3) 试样在NaCl溶液中的腐蚀是阴极控制的活化极化腐蚀,当氧气充分时阴极发生氧去极化过程,除氧之后阴极主要发生氢去极化过程。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808414