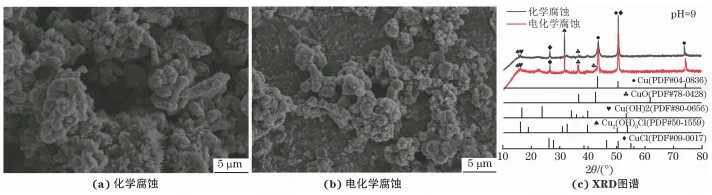
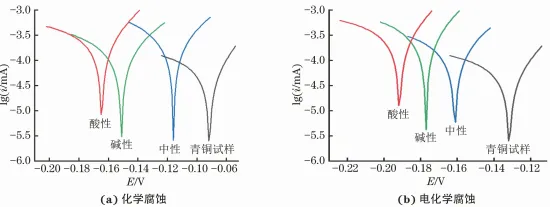
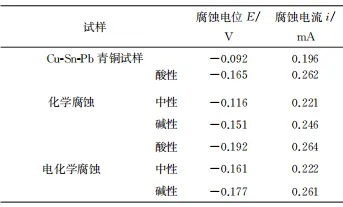
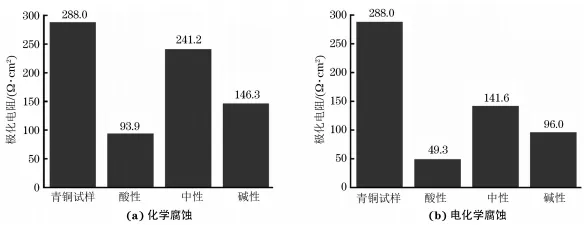
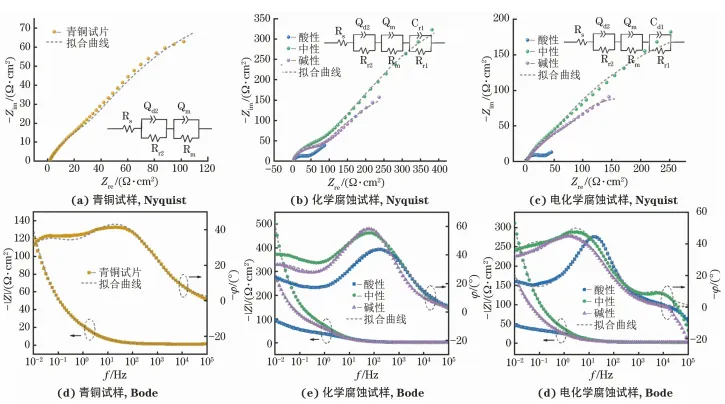
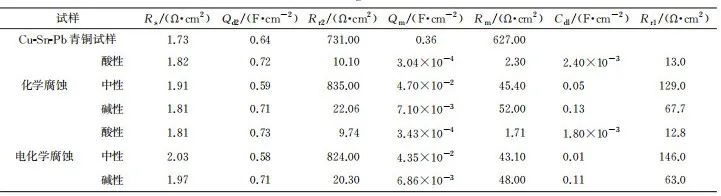
青铜器最早起源于夏王朝时期,在商代至西周前期达到鼎盛,有五千年的历史,是我国古老文明的象征。古青铜器典雅庄重的造型、独特的锈色之美以及岁月的厚重感,使其具有很高的历史价值、艺术价值、文化价值以及科学价值。青铜器深埋于地下成百上千年,在土壤中不可避免会发生不同程度的腐蚀。这会严重损害其历史价值,例如青铜器表面的图案或者铭文遭受腐蚀,重要的考古信息被破坏,甚至导致青铜文物溃烂穿孔,缩短青铜器的寿命。 青铜器是铜、锡、铅三元合金,其金相组织中有铜锡合金的α共熔体和(α+δ) 共析体,且有游离的铅呈不均匀分布,所以青铜器不同微区的电位存在显著差异,会组成若干个微电池,在潮湿环境中极易发生电化学腐蚀,并在表面形成锈蚀产物。其中有害锈又称为“青铜病”,是一种恶性膨胀的铜锈,其发展迅速,对青铜器破坏严重,其危害是各类铜锈之首。“青铜病”在青铜器表面呈现淡绿色,主要由不稳定的氯化亚铜(CuCl)和碱式氯化铜(Cu(OH)3Cl)组成。青铜器在潮湿环境中极易发生腐蚀,除“青铜病”外,还有对青铜器起保护作用的无害锈,其主要成分是氧化铜(CuO)、碱式碳酸铜(Cu2(OH)2CO3) 、以及锡和铅的氧化物等。青铜器的腐蚀取决于青铜器自身的合金成分、组织结构以及埋藏环境。LIANG等研究发现在同一区域出土的青铜器表面锈蚀层是由同种氧化物和不稳定氯化物组成的。SCOTT研究发现不同地区出土青铜器表面的锈色不同,他将其归结为埋藏环境的差异。铁付德研究认为青铜器表面的腐蚀产物与埋藏环境有直接关系,不同器物在同一埋藏环境中的腐蚀程度不同,同种器物在不同埋藏环境中的腐蚀程度也不同。研究者普遍认为青铜腐蚀与青铜器本身的合金成分和埋藏环境中土壤的腐蚀性有关,但是对于不同土壤中出土青铜器的锈蚀状态及腐蚀速率的研究不够深入,也缺乏合适的模拟试验研究方法。 在潮湿环境中,青铜器表面会发生一系列电化学反应,阳极区Cu发生溶解形成Cu+,与环境中Cl-生成不稳定的氯化物,且在青铜器表面发生氧化生成CuO与Cu(OH)2 (CO3)2,阴极区发生氧的去极化反应生成OH-,生成碱式氯化物。青铜器腐蚀是化学或电化学过程,铜锈是铜与环境腐蚀因素化学反应的产物。祝鸿范等通过电化学测试,模拟了青铜器小孔腐蚀的阳极过程,冯丽婷等模拟了青铜器腐蚀的阴极过程,认为氯化亚铜加速多孔氧电极的腐蚀。王菊琳等通过电化学测试研究了青铜器在大气环境中的电化学腐蚀行为。王宁等通过电化学技术研究了青铜试样在不同电解质溶液中的腐蚀行为。以上研究皆表明采用电化学方法研究青铜器的腐蚀行为是可行的。 笔者采用电镀法制备了与古青铜器成分相似的Cu-Sn-Pb青铜试样,在不同pH溶液中获得相应土壤介质出土青铜器的锈蚀产物,并与出土的古青铜器文物表面锈蚀产物的成分进行对比,采用电化学方法研究了相应锈蚀产物的腐蚀行为,以期为青铜器文物的保护研究提供试验基础和科学依据。 1. 1 试剂及仪器 试验所需原料包括焦磷酸钾(K4P2O7)、焦磷酸铜 (Cu2P2O7 )、氢氧化钾(KOH) 、锡酸钠(Na2SnO3)、醋酸铅[Pb(Ac)2] 、氯化铵(NH4Cl)、硫酸铜(CuSO4)和碳酸钠(NaCO3),所有药品均购自上海国药集团,所用试剂均为分析纯,去离子水(DI)为实验室自制。 试验仪器包括X射线衍射仪(XRD) 、场发射扫描电镜(SEM) 、能谱仪(EDS) 、新威BTS400型电池测试设备、电化学工作站(CHI660E) 。 1.2 模拟古青铜器的制备 通过新威BTS400型电池测试设备,采用恒流充电在铜片上电镀Cu-Sn-Pb三元合金, 电镀液成分为 : 175g/LK4P2O7、50mLH2O、34g/LCu2P2O7、25g/LNa2SnO3、4.7g/LPb(Ac)2,采用2.5 g/LKOH溶液调节电镀液pH至8.5~9.0,阴极、阳极接铜片,设置阴极电流密度为15mA/cm2,施镀时间15min,温度55℃,电镀结束后用超纯水、无水乙醇反复清洗试样并将其置于恒温干燥箱中60℃干燥2h,即可得到与古青铜文物成分相似的Cu-Sn-Pb青铜试样。 通过化学方法及电化学方法对Cu-Sn-Pb青铜试样进行腐蚀,模拟不同pH土壤条件下,古青铜器表面的锈蚀状态和产物。腐蚀液由 Mg2SO4、CaCl2、CaSO4按一定比例配制而成,通过添加少量 NaHCO3获得pH分别为5、7、9的腐蚀液,以模拟酸性、中性及碱性土壤介质。化学腐蚀是将Cu-Sn-Pb青铜试样在腐蚀液中浸泡2min,电化学腐蚀则是通过电化学工作站(CHI660E)在相应腐蚀液中对模拟试样进行循环伏安曲线扫描(CV),其中以待腐蚀Cu-Sn-Pb青铜试样为工作电极,饱和甘汞电极为参比电极,铂片为辅助电极, 扫描范围0~-1. 4 V,扫描速率为 0.0035 V/s,灵敏度为 1× 10-4A/V。强制腐蚀结束后用去离子水和乙醇清洗并放入恒温干燥箱中2h,即可得到带锈青铜试样。 1.3 表征与性能测试 采用X射线衍射仪、场发射扫描电镜、能谱仪对Cu-Sn-Pb青铜试样以及强制腐蚀后的试样进行微观形貌观察和结构分析。通过电化学工作站,在3.5%(质量分数,下同)NaCl溶液中测试强制腐蚀后试样的Tafel曲线、阴极极化曲线和电化学阻抗谱(EIS),以带锈青铜试样为工作电极,饱和甘汞电极为参比电极,铂片为辅助电极。Tafel曲线指极化曲线中符合Tafel关系的线性区域,Tafel曲线的扫描范围是相对于开路电位±0.1V。阴极极化曲线指极化曲线的线性极化区域,其斜率可以代表极化电阻的大小。阴极极化曲线的扫描范围是从开路电位到-0.6V,扫描速率为50mV/s。电化学阻抗谱(EIS) 测试频率为10mHz~100kHz,使用ZSimWin软件对阻抗数据进行拟合。 2. 1 Cu-Sn-Pb青铜试样的形貌及成分 由图1可见:通过电镀法,铜片基体上获得了颗粒状物质,该物质由Cu、Sn、Pb三种元素组成,且均匀分布。由图2可见:Cu-Sn-Pb青铜试样的衍射峰分别对应Cu、Cu6Sn5的特征峰,且没有其他杂峰。EDS结果表明,Cu的质量分数为83.30%,Sn的质量分数为15. 2%,而Pb的质量分数仅为1.45%,由于Pb含量较低,在XRD图谱中并没有显示出对应的特征峰。在商代至西周前期,青铜文化达到鼎盛,此时古青铜器的主要成分(质量分数)为:82%~95%Cu、12%~16%Sn、<2%Pb,且Cu、Sn合金以㌳相Cu6Sn5形式存在。因此,通过电镀法制备得到的Cu-Sn-Pb青铜试样与部分古青铜器成分相似。 图1 Cu-Sn-Pb青铜试样的微观形貌及元素分布图 图2 Cu-Sn-Pb青铜试样的XRD图谱和EDS图谱 2.2腐蚀Cu-Sn-Pb青铜试样的形貌及成分 2.2.1 酸性(pH=5)溶液腐蚀 由图3可见:Cu-Sn-Pb青铜试样在酸性溶液中经过化学腐蚀或电化学腐蚀后,表面微观形貌相似,青铜试样表面都生成了形貌疏松,形同粉末的腐蚀产物。XRD结果表明,采用两种腐蚀方式得到的腐蚀产物成分基本一致,主要包括CuO、CuCl和SnO2,这与部分古青铜表面的锈蚀产物成分一致。在酸性溶液中,氧去极化反应生成的大量Cu2+与环境中的O2及Cl-发生相互作用,生成CuO以及不稳定的CuCl。CuCl形貌疏松,水分与O2极易侵入基体,加重腐蚀。Cu-Sn-Pb青铜试样的Sn含量较高,Sn原子易被氧化生成不溶于水的SnO2而富集在Cu-Sn-Pb青铜试样表面。 图3 Cu-Sn-Pb青铜试样在酸性pH=5 溶液中腐蚀后的表面SEM 形貌和XRD图谱 2.2.2 中性(pH=7)溶液腐蚀 由图4可见:在中性溶液中经化学腐蚀后,Cu-Sn-Pb青铜试样表面疏松且有大量孔洞,孔洞周围聚集了大量细丝状和粉末状物质;经电化学腐蚀后,Cu-Sn-Pb青铜试样表面的孔洞周围聚集了大量粉末状物质,且掺杂少量丝状物,查阅参考文献得知,丝状物是铜的氧化物,末状物质是铜的氯化物。王菊琳等利用模拟闭塞电池法研究了青铜器在中性环境中的腐蚀行为,发现青铜器在中性环境中的腐蚀程度较轻,腐蚀产物主要包括铜的氧化物及少量氯化物。XRD结果表明,腐蚀后试样表面生成了CuO、Cu2 (OH)3Cl和CuCl,没有其他的杂峰,该结果与参考文献的描述一致。 图4 Cu-Sn-Pb青铜试样在中性 pH=7 溶液中腐蚀后的表面SEM形貌和XRD图谱 2.2.3 碱性(pH=9)溶液腐蚀 由图5可见:Cu-Sn-Pb青铜试样在碱性溶液中经过化学腐蚀或电化学腐蚀后,表面均发生小孔腐蚀,生成大量疏松状的腐蚀产物,腐蚀产物在小孔周围发生聚集形成孔洞。XRD结果表明,Cu-Sn-Pb青铜试样表面生成的腐蚀产物为 CuO、Cu(OH)2、Cu2(OH)3Cl和 CuCl。胡毅捷等通过分析澄城刘家洼遗址出土青铜器表面的腐蚀产物,发现碱性土壤中出土的青铜器表面锈蚀产物由CuO,以及少量Cu2(OH)3Cl、CuCl等构成。试验结果表明,CuSn-Pb青铜试样在碱性(pH=9)溶液中腐蚀后,表面青铜锈蚀状态和产物与挖掘出土的古青铜器基本一致。以上试验结果进一步证明对Cu-Sn-Pb青铜试样进行化学腐蚀或者电化学腐蚀,可以真实模拟不同土壤介质中出土青铜器的表面状态及产物。 图5 Cu-Sn-Pb青铜试样在碱性 pH=9 溶液中腐蚀后的表面SEM 形貌和XRD图谱 2.3 电化学性能 2. 3. 1 Tafel曲线 由图6和表1可见 : Cu-Sn-Pb青铜试样在3.5%NaCl溶液中的腐蚀电流是0.196mA,而在酸性、中性及碱性溶液中化学腐蚀后,试样的腐蚀电流分别为0.262,0.221,0. 246mA;在酸性、中性及碱性溶液中电化学腐蚀后,试样对应的腐蚀电流分别是0.264,0.261,0.222mA。腐蚀后试样的腐蚀电流均增加,且在酸性溶液中腐蚀后试样的腐蚀电流最大,即其腐蚀速率最大。这是由于酸性介质中氧的去极化反应顺利进行,大量铜发生溶解,与环境中的Cl-生成不稳定的氯化物,由于氯化物疏松多孔,水分子与氧气进入基体并与之发生反应,形成恶性循环,最终导致Cu-Sn-Pb青铜试样腐蚀电流增加,腐蚀加速。 图6 模拟碱性土壤出土青铜试样的极化曲线 表1 Tafel曲线曲线拟合结果 2. 3. 2 极化电阻 由图7可见:Cu-Sn-Pb青铜试样的极化电阻为288.0Ω·cm2,在酸性、中性及碱性溶液中进行化学腐蚀后,其极化电阻分别为93.9,241. 2,146.3 Ω·cm2,在酸性、中性及碱性溶液中进行电化学腐蚀后,极化电阻分别为49.3,141. 6,96. 0 Ω·cm2。腐蚀后Cu-Sn-Pb青铜试样的腐蚀速率均增加,说明腐蚀产物加速了青铜器的腐蚀,无论采用哪种腐蚀方法,腐蚀溶液对Cu-Sn-Pb青铜试样的腐蚀性由强到弱均依次为酸性溶液,碱性溶液,中性溶液。 图7 Cu-Sn-Pb青铜试样及采用不同溶液腐蚀后试样的极化电阻 2. 3. 3 电化学阻抗谱 由图8可见:Cu-Sn-Pb青铜试样及采用不同溶液腐蚀后试样的Nyquist图在高频区均呈现收缩容抗弧,容抗弧可以表征电荷传递的快慢,反映电极材料的耐蚀性。而低频区为Warburg阻抗,表明电极过程受扩散控制,可能是由腐蚀产物膜在金属表面累积引起的。等效电路图中Rs是溶液电阻,Qd2是腐蚀产物生成膜与溶液之间的双层常相位角元件,Rr2是电化学反应的极化电阻,Qm与Rm分别是腐蚀覆盖膜空间电荷层的常相位角元件和电阻,表示反应离子在电场作用下迁移时所受阻力的大小。腐蚀后试样的等效电路图增加一个串联电路,其中Cdl与Rr1分别是腐蚀产物层与铜基体间的双层电容和电化学反应的极化电阻。由表2可见:在酸性、中性及碱性溶液中,化学腐蚀试样的极化电阻Rr2分别是10.10,835.00,22.06Ω·cm2;电化学腐蚀后,试样的Rr2分别为 9. 74, 824. 00, 20. 30 Ω·cm2。极化电阻越大,说明腐蚀程度越小。 图8 Cu-Sn-Pb青铜试样及采用不同溶液腐蚀后试样的电化学阻抗谱 表2 EIS拟合结果 由Bode图可见:在酸性溶液中经电化学腐蚀后,试样的阻抗模量|Z|下降最明显,而在碱性与中性溶液中腐蚀后,试样的|Z|呈现上升状态。Bode图中低频区0.01Hz对应的阻抗模量代表样品的腐蚀程度,阻抗模量越大,腐蚀程度越小。在1~103Hz频率范围内,Bode图相角发生明显下移,且电容回路显著收缩。其中酸性溶液中腐蚀试样的相角下降幅度最大,这是由于酸性溶液中去极化反应的顺利进行,使得大量Cu2+流失,生成不稳定的氯化物与氧化物,且Sn生成氧化物覆盖于试样表面,试样的电阻减小,导电性增加,溶液腐蚀性增强。而在碱性与中性溶液中腐蚀后,试样表面生成致密的氧化层,阻碍了腐蚀反应的进一步进行。 采用化学腐蚀方法,在酸性溶液,中性溶液和碱性溶液中试样的|Z|f=0.01Hz分别为102,509,287Ω· cm2;采用电化学腐蚀方法,在酸性溶液,中性溶液和碱性溶液中试样的|Z|f=0.01Hz分别为52,322,173Ω· cm2。EIS结果表明,Cu-Sn-Pb青铜试样在酸性溶液中的容抗弧半径小于在中性及碱性溶液中的,即在酸性溶液中,Cu-Sn-Pb青铜试样发生的腐蚀最严重,在碱性溶液中的次之,其在中性溶液中的腐蚀最轻。 (1) 采用电镀法制备得到的Cu-Sn-Pb青铜试样与部分古青铜器的成分相似,对青铜试样采用化学腐蚀或电化学腐蚀可以真实模拟不同土壤中出土青铜器的表面锈蚀产物。 (2) 酸性溶液中Cu-Sn-Pb青铜试样的腐蚀最快,碱性溶液中的次之,中性溶液中Cu-Sn-Pb青铜试样的腐蚀最慢。这是因为在酸性溶液中,氧的去极化反应顺利进行,生成大量不稳定的氯化物,腐蚀电流增大,腐蚀加速,这对青铜器造成不可逆的损伤。而在中性和碱性溶液中,Cu-Sn-Pb青铜试样表面被一层较稳定的保护性氧化膜覆盖,腐蚀相对较轻。 (3) 电化学技术在研究金属质文物腐蚀行为中具有重要作用,可为进一步研究青铜器文物保护提供试验基础。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808414