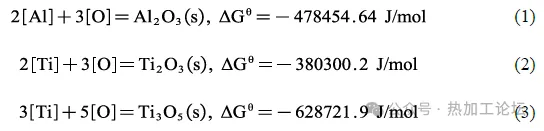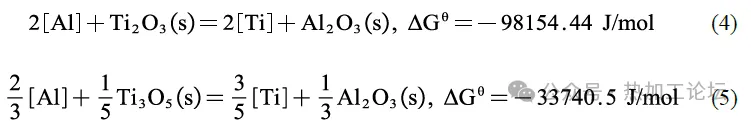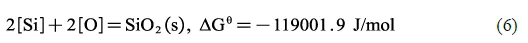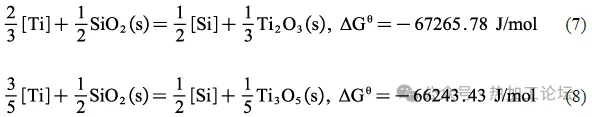钛微合金钢在船舶、航空航天、家电、汽车和建筑等诸多领域有着广泛的应用。向钢中加入Ti 元素进行微合金化,可以提高钢材的强度、改善钢材韧性的各向异性,同时提高耐腐蚀性能和消除回火脆性。在实际生产中,钛微合金钢是在一般碳锰钢及普通高强度低合金钢中添加Ti 元素,后以控轧控冷工艺生产出来的新型钢材。
钛微合金钢的洁净度控制主要体现在对含Ti 夹杂物的控制上。研究结果表明,钢中含Ti 夹杂物主要有TiN、TiC、TiOX 等,大尺寸的含Ti 夹杂物会对钢的力学性能和使用寿命产生极大的危害,同时在生产中堵塞水口影响连铸顺行。但由于Ti 对O有着较强的亲和力,Ti 也被作为重要的脱氧剂使用,近年来Al-Ti 复合脱氧的应用越来越广泛,但是Al-Ti 脱氧钢中生成的大量簇状Al2O3以及大尺寸Al2O3-TiN 夹杂却变得难以控制,此外,Si 元素在钛微合金钢的生产中也参与了脱氧的过程。如何通过复合脱氧工艺的优化设计,进一步提高钢液洁净度,降低有害夹杂物的危害,应是钛微合金钢开发中需要重点关注的研究方向之一。但在目前的研究中,关于钛微合金钢中含Ti夹杂物的生成机理研究尚不明确,对于不同脱氧体系对钢洁净度的影响更是鲜有报道。
基于此,本研究采用热模拟实验和热力学计算相结合的方法,设计了Al-Ti 和Si-Ti两种脱氧体系,对不同体系下的钛微合金钢中含Ti夹杂物的生成行为进行表征分析,总结出不同脱氧顺序对钢中含Ti夹杂物生成的影响,以揭示其生成机理。
1.1 实验钢的制备
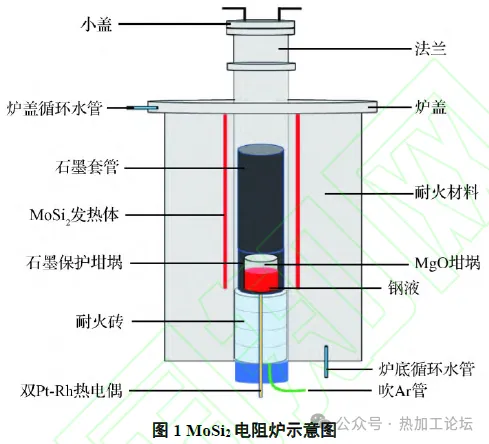
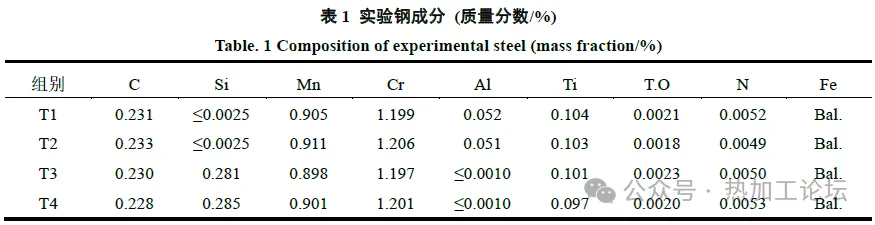
本实验使用MoSi2电阻炉进行实验钢的制备,制备过程中通入99.99%高纯氩气作为保护气,其示意图如图1 所示。同时设计了四组冶炼工艺,图2所示。其中T1组和T2组中Al 的加入量为0.05%,T3 组和T4 组Si 的加入量为0.28%。实验钢的主要化学成分如表1所示。
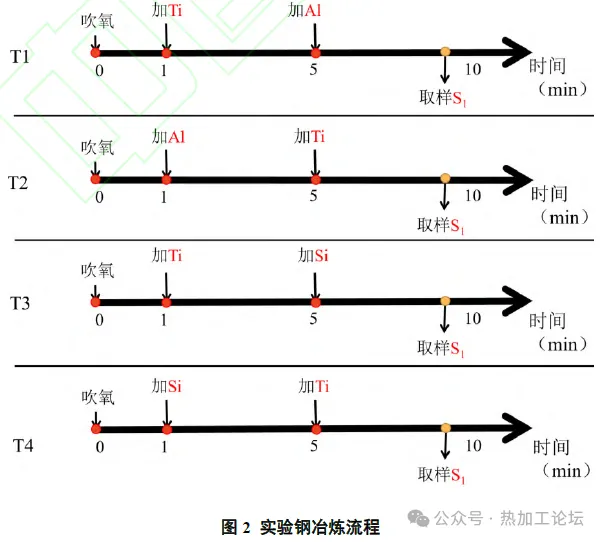
实验开始时使用石英管向钢液中吹氧10s,用以模拟初炼炉冶炼结束时钢水中较高的氧含量,后按照实验流程利用石英管从坩埚中抽取适量钢液,使用水淬方式冷却获得最终样品,并将样品依次命名为T1、T2、T3 和T4。将样品采用线切割的方式制成Φ4mm×7 mm 的圆柱样品。后经打磨抛光获得金相样品,采用扫描电镜-能谱仪(SEM-EDS)和夹杂物自动分析系统(欧波同OTSInca)对样品中的含Ti 夹杂物进行表征分析;采用氮氧分析仪分析样品中O、N含量;采用直读光谱仪分析样品中的主要合金成分。
2.1 不同脱氧顺序对钢中夹杂物的影响
2.1.1 Al 脱氧体系下不同脱氧顺序对含Ti 夹杂物的影响 使用SEM-EDS分别对先Ti 后Al(T1)和先Al 后Ti(T2)得到的实验钢中的夹杂物进行观察分析,其典型形貌分别如图3和图4所示。
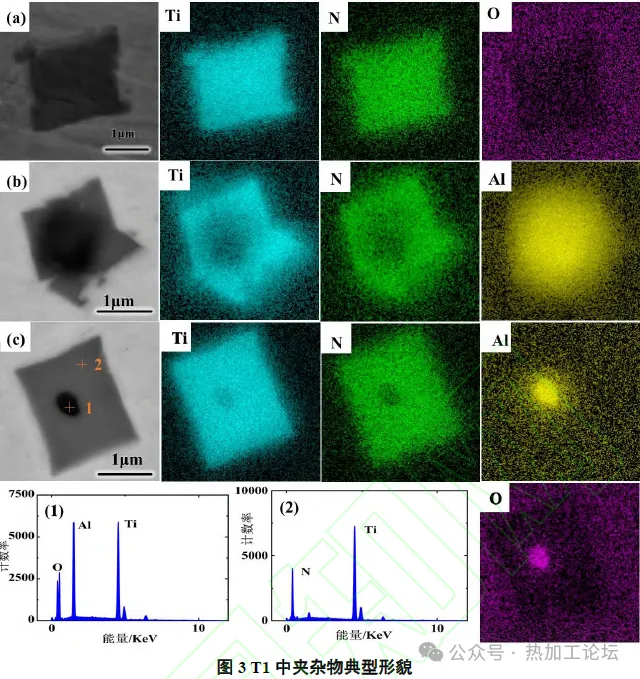
由图3可知,T1中的夹杂物主要为方形的TiN夹杂(2~3μm)和棱角分明的Al2O3-TiN 复合夹杂(3~4 μm)。结合图3(c)以及能谱图(1)、(2)的表征结果可知,Ti 的含量在整个复合相的中心和四周均有分布且不均匀,中心形成的Al-Ti-O 复合夹杂物处Ti 含量较低,外部TiN 的Ti 含量较高。
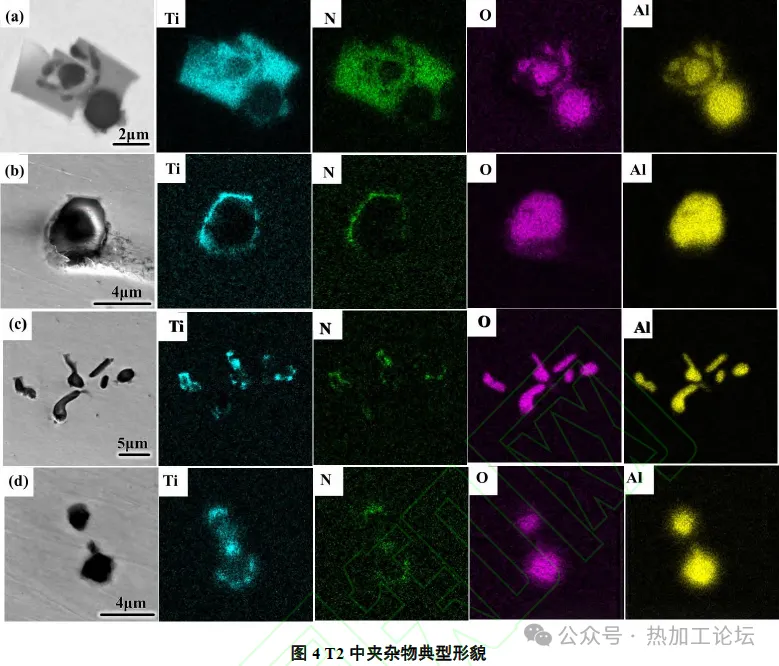
由图4可知,T2中夹杂物主要有TiN、Al2O3-TiN复合夹杂以及大量簇状的Al2O3夹杂。其中Al2O3-TiN复合夹杂的形态多样,但总体分为三类,第一类为Al2O3外围包裹大尺寸方形TiN的复合夹杂(≥5μm);第二类为大尺寸Al2O3外围包裹一层薄的TiN 的近圆形复合夹杂物(2~4 μm);第三类为以簇状Al2O3为核心,外部包裹TiN 的复合夹杂物(≥5μm)。这三类夹杂物虽然都为Al2O3-TiN复合夹杂,表现为TiN以Al2O3为形核质点生成,但形貌却有着明显的差异,这是因为先添加Al 使钢中首先生成大量形态不一的Al2O3所造成的,这种结果同先加Ti 后加Al 时生成的Al2O3-TiN 复合夹杂形成较为明显的区别。通过对比几种Al2O3-TiN 复合夹杂,可以看出TiN 包裹层的尺寸随Al2O3核心层尺寸的大小而变化。当Al2O3核心层尺寸较大时,TiN 包裹层尺寸相对较小;当Al2O3核心层尺寸较小时,TiN 包裹层尺寸则相对较大。这是因为当夹杂物以异质形核方式生成时,形核核心的半径越大,外层夹杂形核所需要的形核功越大,就越不容易形核。此时钢中大量的Ti、N 原子将依附在尺寸相对较小的Al2O3上形核,这就造成了Al2O3-TiN 复合夹杂在钢中以多种尺寸形态存在的结果。 对比分析Al-Ti 脱氧体系下的两组结果,发现两组钢中均未明显观察到TiOX,这是因为Al与O的亲和力要强于Ti,先加入Al 时,Al和钢液中的O 反应生成Al2O3,当钢液中有足够的溶解Al 时,钢液中的O与Al平衡,受Al 控制,使得O 几乎不与Ti 反应结合生成Ti 的氧化物。此外,在先加Ti 后加Al 时,钢中最先生成少量TiOX,但随着Al的加入,O更易与Al结合,钢液中的复杂脱氧反应向着生成Al2O3这种更稳定相的方向进行,且还存在少量Al 向着TiOX 夺O的反应,导致钢中最先生成的TiOX 变少,使得钢中最终稳定存在的氧化物相为Al2O3,其机理如(1)-(5)式所示。由式(4)、(5)可知,因此不论Al、Ti 的加入顺序如何,钢中最稳定的相应为Al2O3,这与实验表征结果一致。
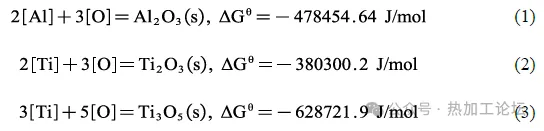
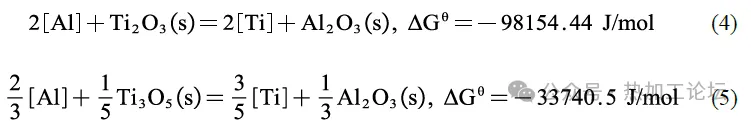
2.1.2 Si 脱氧体系下不同脱氧顺序对含Ti夹杂物的影响 分别对先Ti 后Si(T3)和先Si 后Ti(T4)得到的实验钢中的夹杂物进行观察分析。其典型形貌分别如图5和图6所示。
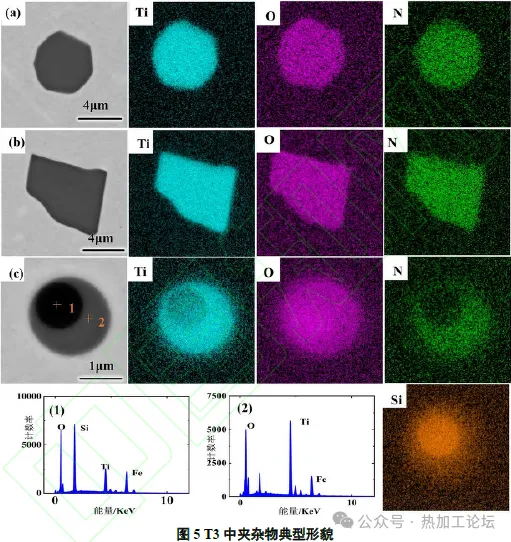
由图5 可知,钢中含Ti 夹杂物的种类较Al-Ti 脱氧体系中变得丰富,出现了近圆形和近方形的Ti-O-N复合夹杂(≥5μm)以及圆形SiO2-TiN 复合夹杂(2~3μm)。对图5(c)夹杂物中心及外围打点进行能谱分析,结果如图5(1)、(2),可以看出这类夹杂物为SiO2-TiOX 复合夹杂。
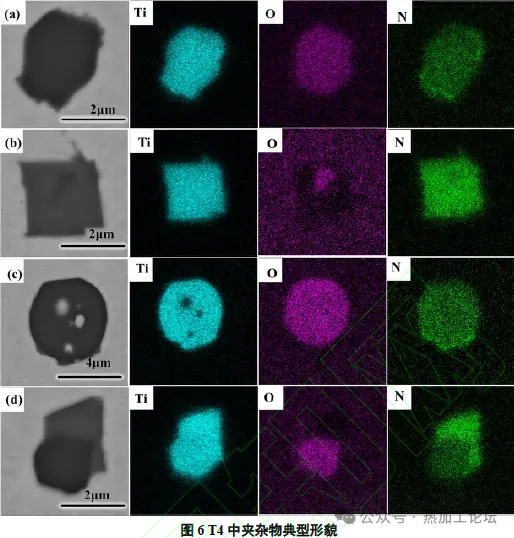
由图6 可知,T4 中有长条形的TiOX(4~5μm)以及Ti-O-N 复合夹杂物(3~4μm)生成。Ti-O-N 复合夹杂物有两种类型,且尺寸无明显差异,一种夹杂物中Ti、N、O 元素均匀分布,而另一种则是以TiOX 为形核质点的TiOX-TiN复合夹杂。 在Si-Ti 复合脱氧的两组实验中,含Ti 夹杂物主要是Ti-O-N 系复合夹杂。通过对比T3 的结果还可以看出,Ti、Si 加入顺序的变化导致T4 中的含Ti 夹杂物尺寸要明显比T3小。此外,在先加Si 后加Ti 时,钢中虽然出现了大量TiOX-TiN 复合夹杂,但未出现SiO2,这与T3 的表征结果产生了明显的差异。这是因为在1600℃时,在T3实验钢中,Ti首先脱去了钢中大部分的O,残余O 与后加入的Si 形成了少量了SiO2,此时钢中剩余的少量溶解Ti与SiO2 发生如式(7)、(8)的反应,但由于剩余的Ti 含量过少,不能完全将SiO2 转化为Ti 的氧化物,所以最终形成了SiO2-TiOX 的复合结构。而在T4中,先加入的Si与O先反应生成SiO2,其反应的Gibbs 自由能如式(6)所示,后加入Ti时,钢中发生如式(2)、(3)所示的反应。结合式(2)、(3)和(6)可得到式(7)、(8),由式(7)、(8)可知,因此在后加入Ti 时,钢中的最稳定相由SiO2 转变为TiOX,这与实验表征的结果一致。因此,Si、Ti 的加入顺序不仅影响了钢中含Ti 夹杂物的尺寸,更影响了种类。
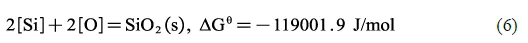
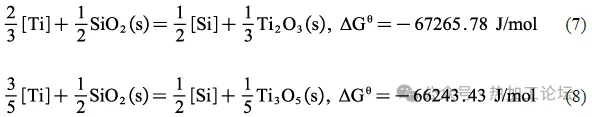
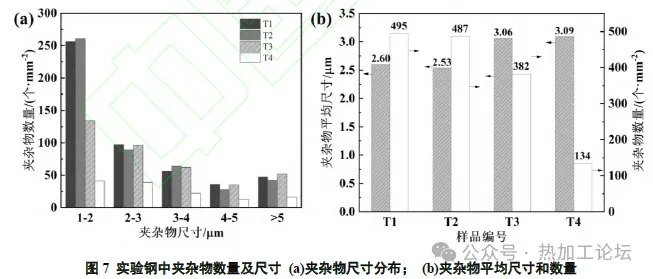
四组实验钢中夹杂物数量及尺寸分布如图7所示。由图7(a)可知,T1 和T2 钢中夹杂物尺寸分布相近,大部分夹杂物分布在1~2μm 之间;T3 与T4 钢中夹杂物尺寸分布相似且在不同尺寸内的分布较为平均,大部分夹杂物分布在2~4 μm 之间。由图7(b)可知,T1、T2、T3 和T4 中夹杂物平均尺寸分别为2.60 μm、2.53 μm、3.06 μm 和3.09 μm,夹杂物数密度从T1~T4 依次减小。可以发现,Al-Ti 脱氧体系下夹杂物的数密度大于Si-Ti 脱氧体系,但夹杂物平均尺寸却小于Si-Ti 脱氧体系,这说明Al-Ti 脱氧体系下的夹杂物更加细小弥散,而Si-Ti 脱氧体系中的夹杂物更加粗大。从图中还可以看出,1~2 μm区间内T1 和T2 夹杂物数量远大于T3 与T4,而在2~5 μm 区间内,T1、T2 及T3 夹杂物数量相差较小,其中T4 在各个尺寸的夹杂物数量都是最少的。因此,从夹杂物尺寸控制的角度来看,先加Al 后加Ti 的脱氧方式对夹杂物的细化效果最好;而从夹杂物数量控制的角度来看,先加Si 后加Ti 的脱氧方式中的夹杂物数量最低。
为了探究不脱氧体系下Al、Ti、Si 的含量变化分别对夹杂物生成的热力学条件的影响,分别将Al、Ti、Si 的含量设置为梯度变量,并基于FactSage 8.2 中的Equilib 模块及FactPS、FSstel 数据库对实验钢进行热力学模拟计算,计算方案如表2 所示。
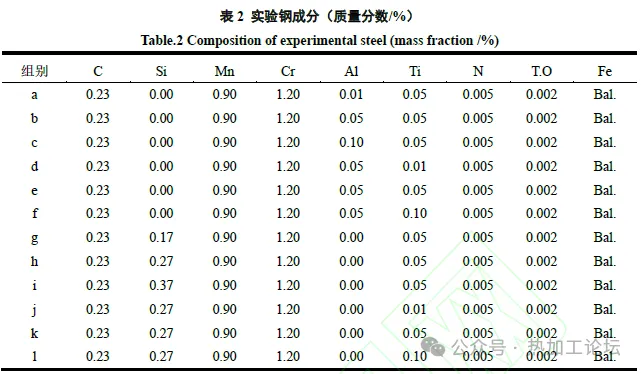
2.3.1 Al 脱氧体系下不同Al、Ti 含量对夹杂物生成的影响 Al含量的变化会对含Ti 夹杂物的种类、数量以及形态产生影响。因此,选取a、b、c、d、e、f 组做热力学计算,考察不同Al、Ti 含量对钢中夹杂物生成的影响,其中a、b、c 组Ti 质量分数为0.05%,而Al 的质量分数为0.01%、0.05%和0.10%;d、e、f组Al 质量分数为0.05%,而Ti 的质量分数为0.01%、0.05%和0.10%,计算结果如图8所示。
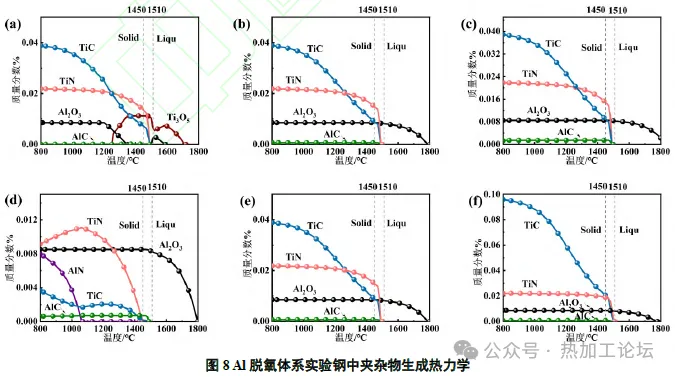
由图8 可以看出,Al 脱氧体系中,存在明显的Al2O3→TiN→TiC 的生成顺序,这是导致Al2O3-TiN 复合夹杂生成的原因。同时,TiN 和TiC 的初始生成温度(1500 ℃左右)不随Al、Ti 含量变化而变化,最大生成量只随着Ti 含量增加而增加,TiOX 只在Al 含量为0.01%时有少量生成,但最终氧化产物都为Al2O3,并且Al2O3的最大生成量稳定不变。这是因为钢液中Al 与Ti 存在着竞争O 的关系,在Al 含量较少时,Ti 与O 结合的趋势更大,先形成TiOX,随温度下降,Al2O3开始生成,并同时竞争TiOX中的O,导致TiOX 逐渐消失,脱离出的O与Al结合为Al2O3,Al 的含量达到一定值后,钢中只生成Al2O3,不再生成TiOX,由于钢液中O的含量是一定的,所以Al2O3的最大生成量是一定的。Al 含量较大时,Al2O3在钢液中的形核更具有优势,在高温时直接形成稳定的Al2O3,大量Al2O3可以为TiN形核提供形核核心,此结果与热模拟实验一致。2.3.2 Si 脱氧体系下不同Si、Ti 含量对夹杂物生成的影响 选取g、h、i、j、k、l 组做热力学计算,考察不同Ti、Si 含量对钢中夹杂物生成的影响,其中g、h、i 组Ti 质量分数为0.05%,而Si 的质量分数为0.17%、0.27%和0.37%;j、k、l 组Si 质量分数为0.27%,而Ti 的质量分数为0.01%、0.05%和0.10%,计算结果如图9 所示。
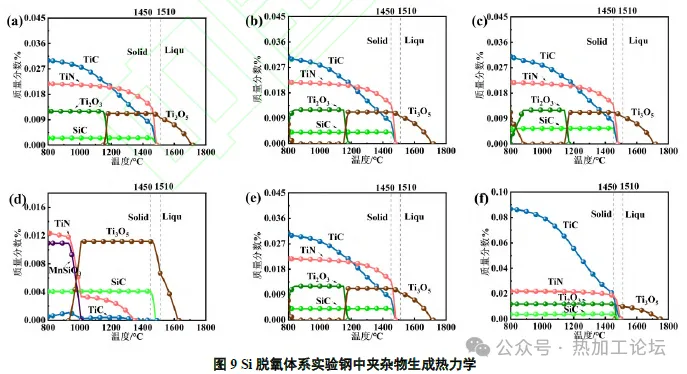
由图9 可以看出,Si 脱氧体系中,存在Ti3O5→TiN→TiC→Ti2O3 的生成顺序,这是导致TiOX-TiN 复合夹杂生成的原因。但在计算中发现没有SiO2 生成,这是因为模拟计算是在理想条件下进行的,而实验中加入合金到取样的时间较短,同时采用了水淬取样的方式,这势必会影响SiO2 生成的热力学和动力学条件,因此模拟计算与实验之间存在了差异。 此外,TiC 和SiC 的初始生成温度(1500℃左右)不随Si、Ti 含量变化而变化,但TiC最大生成量随Ti 含量增加上升,而SiC 最大生成量基本保持不变。TiN(约1500℃)、Ti2O3(约1170℃)和Ti3O5(约1750℃)的初始生成温度不随Si含量变化而变化,但随着Ti含量增加,TiN的初始生成温度从1350 ℃左右上升至1500℃左右,Ti3O5的初始生成温度从1650℃左右上升至1800 ℃左右。Ti3O5的最终生成量随着Si 含量增大而增大,而Ti2O3 的最终生成量随着Ti含量增大而增大,两者之间的转变温度(1200℃左右)不随Si 含量变化而变化,但随Ti 含量增加而增大至1500 ℃左右。当Ti 含量升高时,钢中的O与Ti几乎全部生成TiOX,剩余Ti与N 结合形成TiN,由于Ti3O5 开始生成温度大于TiN,故Ti3O5 在冷却过程中先生成。而当Ti 含量较高时,TiN 的生成温度与Ti3O5 和Ti2O3 的转变温度相近,所以存在一部分夹杂物为元素均匀分布的Ti-O-N复合夹杂,另一部分为TiOX-TiN复合夹杂的可能。
(1)Al、Ti、Si 对O 的亲和力依次下降,Al2O3、TiOX 和SiO2 都可以作为形核核心诱导含Ti 夹杂物(TiN、TiOX)形核,形成的含Ti 复合夹杂物的形貌由方形逐渐向圆形转变。从夹杂物尺寸控制来看,先加Al 后加Ti 的脱氧方式对夹杂物的细化效果最好(约为2.53μm);从夹杂物数量控制来看,先加Si 后加Ti 的脱氧方式中的夹杂物数量最低(约为134/mm-2)。
(2)Al 脱氧体系中,存在Al2O3 → TiN → TiC 的生成顺序,大量Al2O3 的生成抑制了TiOX 生成。Si 脱氧体系中,存在Ti3O5→TiN→TiC→Ti2O3 →SiO2 的生成顺序,1200℃左右Ti3O5逐渐转变为Ti2O3。(3)Al2O3-TiN 复合夹杂物中,TiN 包裹层的尺寸随Al2O3 核心层尺寸的大小而变化,当Al2O3 核心层尺寸较大时,TiN 包裹层尺寸相对较小;当Al2O3 核心层尺寸较小时,TiN 包裹层尺寸则相对较大。