摘要
通过化学镀技术制备Ni-Cr-P三元合金镀层。利用称重法,SEM,EDS,XRD和电化学测试等方法,研究镀液中CrCl3,C3H6O3,C2H5NO2和K2C2O4浓度对Ni-Cr-P镀层的沉积速率、Cr含量及其在模拟燃料电池环境中电化学腐蚀行为的影响。结果表明,CrCl3浓度增加,沉积速率提高;随着C3H6O3,C2H5NO2和K2C2O4浓度的增加,沉积速率不断降低。Ni-Cr-P镀层的表面形貌呈胞状结构,镀层为非晶和微晶混合结构。Ni-Cr-P镀层的自腐蚀电位远高于Ni-P二元合金镀层的,向正移动约0.25 V;其电荷转移电阻增大,腐蚀电流密度降低了约两个数量级,Ni-Cr-P三元合金镀层的耐蚀性明显优于Ni-P二元合金镀层的。
关键词: 化学镀; Ni-Cr-P合金镀层; 配位剂; 电化学阻抗; 极化曲线
近几年,化学镀Ni-W-P[1],Ni-Sn-P[2],Ni-Cu-P[3],Ni-Fe-P[4],Ni-Mo-P[5]的研究已经取得了很大的进步,获得了性能更加优异且能满足不同场合要求的镍基合金镀层[6,7,8,9]。但是,通过化学镀的方法沉积Ni-Cr-P三元合金镀层的研究相对较少[10,11]。由于Cr在空气和水中都相当稳定,表面容易形成一层氧化膜而变为钝态。有研究[12,13]证明,含Cr量仅为0.1% (质量分数) 化学镀Ni-Cr-P合金镀层的耐蚀性明显优于Ni-P二元合金的;又有研究[14,15]证明,Cr的共沉积使镀层提前进入非晶态,非晶态合金具有优异的磁性、耐磨性、高强度、硬度和韧性等。而Ni-Cr-P合金形成非晶所需的P含量低于Ni-P合金的,说明Cr的存在有利于非晶结构的形成,Cr富集在镀层外表面,使镀层的自钝化倾向加强,耐蚀性显著提高[16,17]。
此外,化学镀Ni-Cr-P三元合金具有较小的电阻温度系数 (TCR),适用于电子零部件的表面处理。化学镀Ni-Cr-P恰好弥补了电镀铬制作成本高、镀层厚度薄、环境污染严重等缺点[18,19]。
由于Cr与Ni共沉积困难,镀液的组成和pH值不断变化,所以Ni-Cr-P化学镀层制备困难较多。目前,关于化学镀Ni-Cr-P的制备与腐蚀行为的报道比较少。本工作对化学镀法制备的Ni-Cr-P三元合金镀层在模拟燃料电池环境 (0.5 mol·L-1硫酸溶液) 中电化学腐蚀行为进行研究,探讨镀液中CrCl3,C3H6O3,C2H5NO2和K2C2O4浓度对Ni-Cr-P三元合金镀层的沉积速率、Cr含量及其耐腐蚀性能的影响。
1 实验方法
本实验选用的基体材料为Q235钢,规格为12.5 mm×20 mm×0.8 mm。其化学成分 (质量分数,%) 为:C 0.14~0.22,Mn 0.30~0.65,Si≤0.30,S≤0.050,P≤0.045,Fe余量。化学镀之前,依次对试样进行砂纸打磨→称重→超声波除油→水洗→酸洗除锈→水洗→活化→水洗处理。之后,将样品放入化学镀溶液中进行施镀。化学镀Ni-Cr-P镀液基础配方的主要成分为:10 g·L-1 NiSO4,10 g·L-1 NaH2PO2,10 g·L-1 Na3C6H5O7,5 g·L-1 CrCl3,5 g·L-1 CHKO2,1 mg·L-1 CH4N2S,pH值为4.6,温度85 ℃,施镀时间为1 h。
采用S3400型扫描电子显微镜 (SEM) 观察镀层的微观形貌,并用附带的X射线能谱仪 (EDS) 测试镀层中Cr的含量 (质量分数)。采用MiniFlex600型X射线粉末衍射仪 (XRD) 测试镀层的晶相结构,CuKα辐射,管电流15 mA,电压40 kV,扫速8 °/min。
采用称重法计算镀层的沉积速率,计算公式如下:

式中,v为沉积速率,μm·h-1;m1和m2分别为施镀前后试片质量,g;ρ为镀层质量密度,g·cm-3;s为试片面积,cm2;t为化学镀时间,h。所有实验均测试3个平行试样。
电化学测试采用CHI604E电化学工作站。电解池为三电极体系,工作电极为浸泡在电解液中暴露面积为1 cm×1 cm的化学镀样品,辅助电极为Pt电极,参比电极为饱和甘汞电极。电解液为0.5 mol·L-1的硫酸溶液。极化曲线测试电位范围为自腐蚀电位±150 mV,扫描速率为0.5 mV·s-1。极化曲线实验结果采用CHI604E电化学工作站自带分析软件进行分析。电化学阻抗测试在开路电位下进行,扰动信号的幅值为5 mV,频率范围为105~10-2 Hz,扫描方向由高频至低频,阻抗实验结果采用ZSimpWin软件进行拟合分析。
2 结果与讨论
2.1CrCl3浓度对镀层沉积速率和耐蚀性的影响
通过在化学镀Ni-P合金基础配方中加入CrCl3,来制备Ni-Cr-P三元合金镀层。镀层中Cr含量利用SEM附带的EDS进行测定。图1为化学镀液中的CrCl3浓度对镀层沉积速率和镀层中Cr含量的影响。可以看到,随着CrCl3浓度的增加,沉积速率逐渐增大;当CrCl3浓度为20 g·L-1时,沉积速率达到最大。值得注意的是,CrCl3浓度为20 g·L-1时,镀液出现了分解,这可能是由于配位剂的含量不足导致的,表明在配位剂浓度一定的条件下,镀液中的CrCl3浓度不宜过高。而当CrCl3浓度低于5 g·L-1时,镀层外观较差;当浓度大于15 g·L-1时,镀层外观也较差;浓度在5~15 g·L-1时镀层的外观良好,这与文献[14]的结果基本一致。由图1可知,镀层中Cr含量均小于1%,这与文献[16]报道的结果相似。当CrCl3浓度为3 g·L-1时,镀层表层中几乎不含Cr;当CrCl3浓度为5 g·L-1时,Cr的含量为0.64%;当CrCl3浓度大于5 g·L-1时,镀层中Cr的含量逐渐变小,这可能与镀液不稳定并且分解有关。
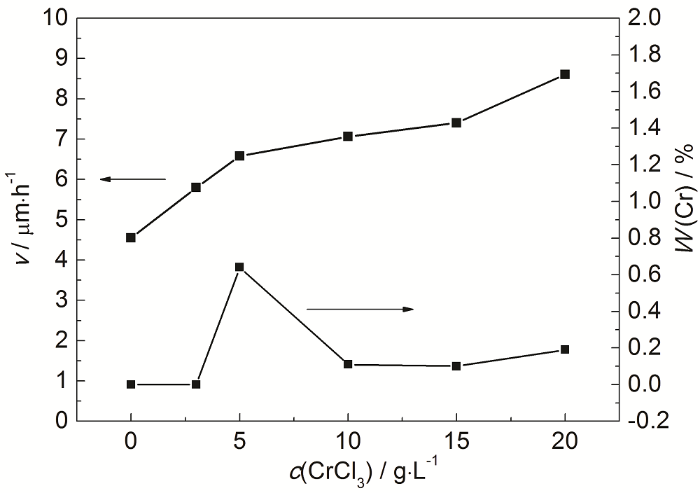
图1 镀液中CrCl3浓度对镀层沉积速率和Cr含量的影响
图2a为在不同CrCl3浓度的镀液中所制备Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的极化曲线,表1为图2的极化曲线和EIS拟合参数。由图2a和表1可以看出,CrCl3浓度对镀层的自腐蚀电位有影响,CrCl3浓度为20 g·L-1时,所制备的Ni-Cr-P镀层的自腐蚀电位 (Ecorr) 较负,其腐蚀电流密度 (Icorr) 较大;而在其他浓度下所制备Ni-Cr-P镀层的自腐蚀电位相对较正并且相差不大,腐蚀电流密度也相差不大。当CrCl3浓度为5 g·L-1时,所制备镀层的腐蚀电流密度较小,为6.971 μA·cm-2。由于极化电阻 (Rp) 与腐蚀电流密度成反比,此时对应的极化电阻较大,为6019 Ω·cm2。表明此镀层具有较好的耐蚀性能,这可能与在该条件下Cr含量相对较高有关。

图2 不同CrCl3浓度条件下Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的动电位极化曲线和电化学阻抗谱
表1 Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的极化曲线和EIS拟合参数
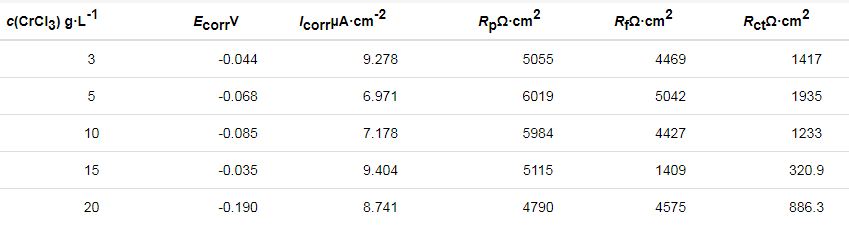
图2b为在不同浓度的CrCl3镀液中所制备的Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的Nyquist图及选用的等效电路图。结果表明,Nyquist图中均出现了明显的容抗弧,在高频区的容抗弧表明与镀层腐蚀相对应的电极反应受电化学反应控制,这与镀层在0.5 mol·L-1硫酸溶液中的腐蚀行为相对应;在中频和低频区的半径大小可能与镀层在溶液中的腐蚀产物膜阻抗的大小以及其保护镀层的性能有关[20]。采用R(Q(R(CR))) 等效电路图对结果进行拟合。其中,Rf为镀层在0.5 mol·L-1硫酸溶液中的腐蚀产物膜电阻,Rct为电荷传递电阻。电化学阻抗谱 (EIS) 拟合的部分参数值 (Rf和Rct) 列在表1中。Rf和Rct的数值越大,表明其镀层的耐蚀性越好。由表1可知,当CrCl3浓度为5 g·L-1时所制备的镀层的Rf为5042 Ω·cm2,Rct为1935 Ω·cm2,其数值均较大,这与采用极化曲线拟合的结果基本一致。
2.2 C3H6O3浓度对镀层沉积速率和耐蚀性的影响
C3H6O3是化学镀Ni-P合金最常用的配位剂之一。图3为C3H6O3浓度对沉积速率和镀层中Cr含量的影响。可以看到,随着C3H6O3浓度的增高,镀速逐渐下降,原因可能是随着C3H6O3浓度增加,其配位作用逐步加强,此时配位剂与金属离子形成稳定的配合物。而过多的配位剂与活性Ni2+配合,减小了游离Ni2+的浓度,因此Ni的还原沉积过程受到影响,被还原的Ni2+数目减少,沉积速率降低。Ni的还原速度在一定程度上也会影响Cr的还原速度[21]。由图3可以看到,加入C3H6O3后,Cr的含量相比不加C3H6O3时有下降,改变C3H6O3浓度对镀层中Cr含量影响不大,而乳酸加入可以明显增加三元镀液的稳定性。
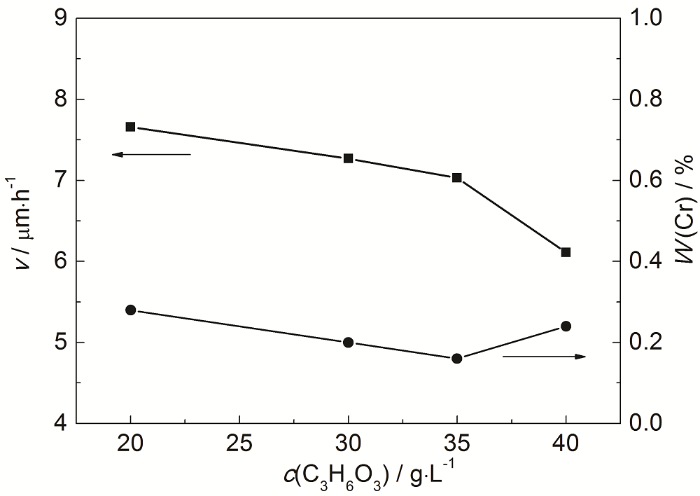
图3 C3H6O3浓度对沉积速率和Cr含量的影响
图4a是不同浓度C3H6O3镀液中所制备的Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的极化曲线,表2为图4极化曲线和EIS的拟合参数。由表2可知,改变C3H6O3浓度对所制备的镀层的耐蚀性影响不大;当C3H6O3浓度为20 mL·L-1时,镀层的耐蚀性相对最好,腐蚀电流密度为7.178 μA·cm-2。
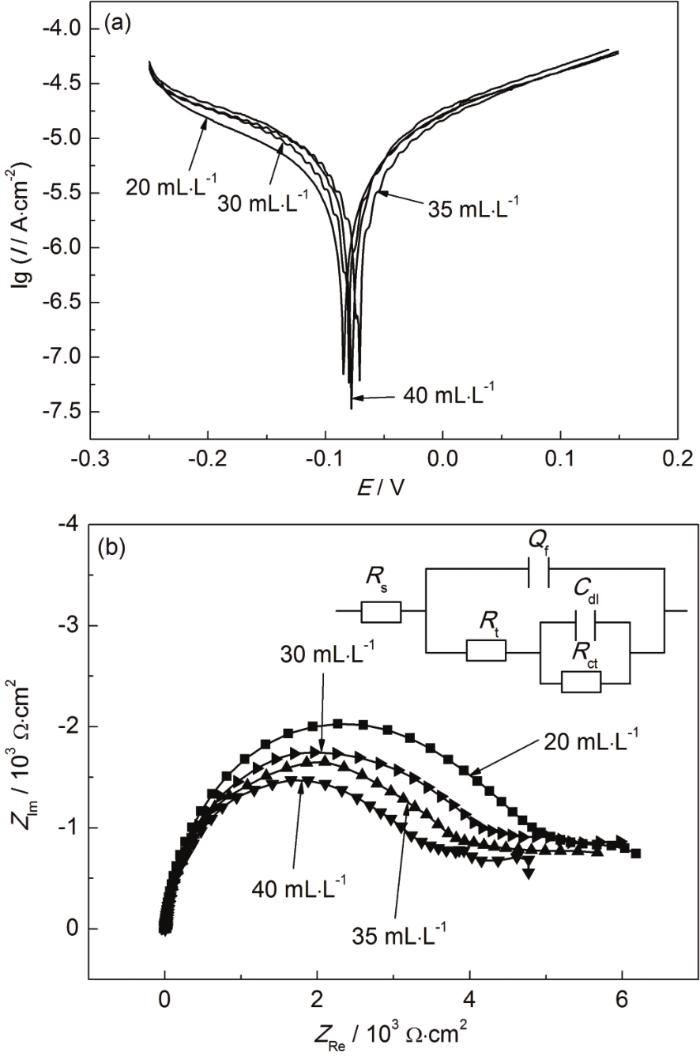
图4 不同浓度C3H6O3条件下Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的动电位极化曲线和电化学阻抗谱
表2 Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的极化曲线和EIS拟合参数

图4b为是不同浓度C3H6O3镀液中所制备的Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的Nyquist图及选用的等效电路图。采用R(Q(R(CR))) 等效电路图对结果进行拟合。电化学阻抗谱 (EIS) 拟合的部分参数值列在表2中。Rf和Rct的数值越大,表明其耐蚀性越好。当C3H6O3浓度为20 mL·L-1时,所制备的镀层的Rf为4367 Ω·cm2,Rct为1106 Ω·cm2,其数值均较大。改变镀液中C3H6O3的浓度,对所制备镀层的耐蚀性影响不大,其影响规律和采用极化曲线拟合的结果基本一致。通常,在单一乳酸体系的Ni-P二元合金镀液中所制备镀层的耐蚀性一般不够理想,而加入其他配位剂可以改善镀层的耐蚀性[22]。
2.3 C2H5NO2浓度对镀层沉积速率和耐蚀性的影响
C2H5NO2是一种较弱的Ni、Cr离子的配位剂,金属离子与配位剂的弱配位是从化学镀溶液中获得高质量镀层的要求之一[11,19]。在化学镀Ni-P二元合金镀液中,C2H5NO2能显著提高镀层沉积速率且改善外观[22]。图5为其它添加剂浓度不变的情况下,C2H5NO2浓度对镀层沉积速率和Cr含量的影响。可以看到,随着C2H5NO2浓度的增加,镀速下降,这与对二元合金镀层的影响规律不同;当C2H5NO2的浓度为0.1 g·L-1时,镀速最大,这个浓度范围与C2H5NO2对二元化学镀Ni-P合金中的影响一致。在化学镀Ni-P二元合金中,C2H5NO2的用量一般小于1 g·L-1。当C2H5NO2的浓度为4 g·L-1时,镀层中Cr的含量为0.36%;C2H5NO2浓度为15 g·L-1时,Cr的含量较低,这可能是C2H5NO2浓度对Ni的沉积有较大影响造成的。
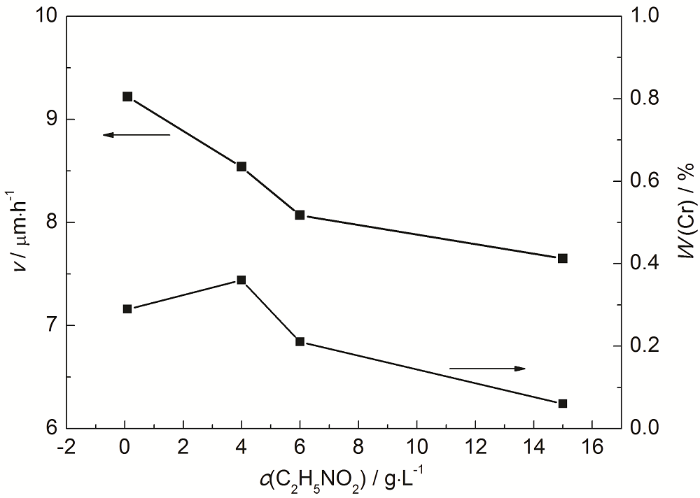
图5 甘氨酸浓度对沉积速率和Cr含量的影响
图6a是不同浓度C2H5NO2镀液中所制备的Ni-Cr-P镀层的极化曲线图,表3为图6的极化曲线和EIS拟合参数。由图6a和表3可知,当C2H5NO2浓度为6 g·L-1时,镀层的耐蚀性最好,腐蚀电流密度为7.787 μA·cm-2。

图6 不同C2H5NO2浓度条件下Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的动电位极化曲线和电化学阻抗谱
表3 Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的极化曲线和EIS拟合参数
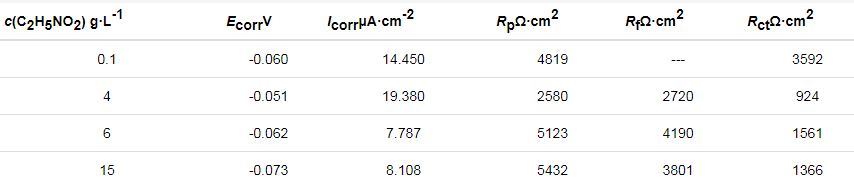
图6b为不同浓度C2H5NO2镀液中所制备的Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的Nyquist图及选用的等效电路图。采用R(Q(R(CR))) 等效电路图对结果进行拟合。EIS的拟合参数值列在表3中。当C2H5NO2浓度为6和15 g·L-1时所制备的镀层的Rf和Rct的数值均较大,Rf和Rct的数值越大,表明其耐蚀性越好,这与采用极化曲线拟合的结果基本一致。在文献[11]中,浓度为15 g·L-1的甘氨酸作为Cr3+的配位剂与柠檬酸钠复配,可以获得耐蚀性较好的三元镀层。
2.4 K2C2O4浓度对镀层沉积速率和耐蚀性的影响
K2C2O4在碱性体系中通常作为Cr3+的主配位剂[7,8,9,10],而在酸性体系中则较少采用。图7为K2C2O4浓度对镀层沉积速率和镀层中Cr含量的影响。可以看到,随着K2C2O4浓度的增加,沉积速率逐渐下降。由于Cr3+的配位剂通常为羟基羧酸及其盐,如甲酸和乙酸盐、氨基乙酸、草酸及其盐、柠檬酸及其盐、硫氰酸盐和酒石酸盐等,其与Cr3+配位顺序大致为:CNS-<HCOO-<CH3COO-<C4H4O42-<C4H4O62-<C2H3O3-=C3H5O3-<C3H2O42-<C6H7O7-<C2O42-<OH-[23]。可见K2C2O4与Cr的配位能力很强,而且从图中可以看出,随着K2C2O4含量的增加,沉积速率逐渐下降,这是因为K2C2O4的含量增多,与Ni2+和Cr3+充分配合,使其配合物极其稳定,NaH2PO2不能将其还原,导致沉积速率降低。K2C2O4含量对镀层成分影响不大。当K2C2O4为2.5 g·L-1时,镀层中Cr的含量为0.30% (质量分数)。K2C2O4的加入也改善了三元镀液的稳定性。
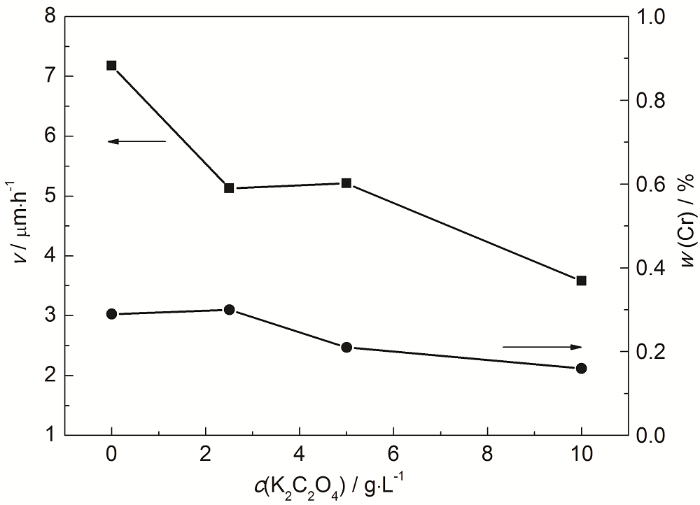
图7 K2C2O4浓度对沉积速率和Cr含量的影响
图8a是不同浓度K2C2O4镀液中所制备的Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的极化曲线,表4为图8的极化曲线和EIS拟合参数。由表4可以看出,当K2C2O4浓度为2.5 g·L-1时,腐蚀电位较正,镀层的耐蚀性相对较好,腐蚀电流密度为4.849 μA·cm-2,K2C2O4的加入对镀层耐蚀性影响较大。
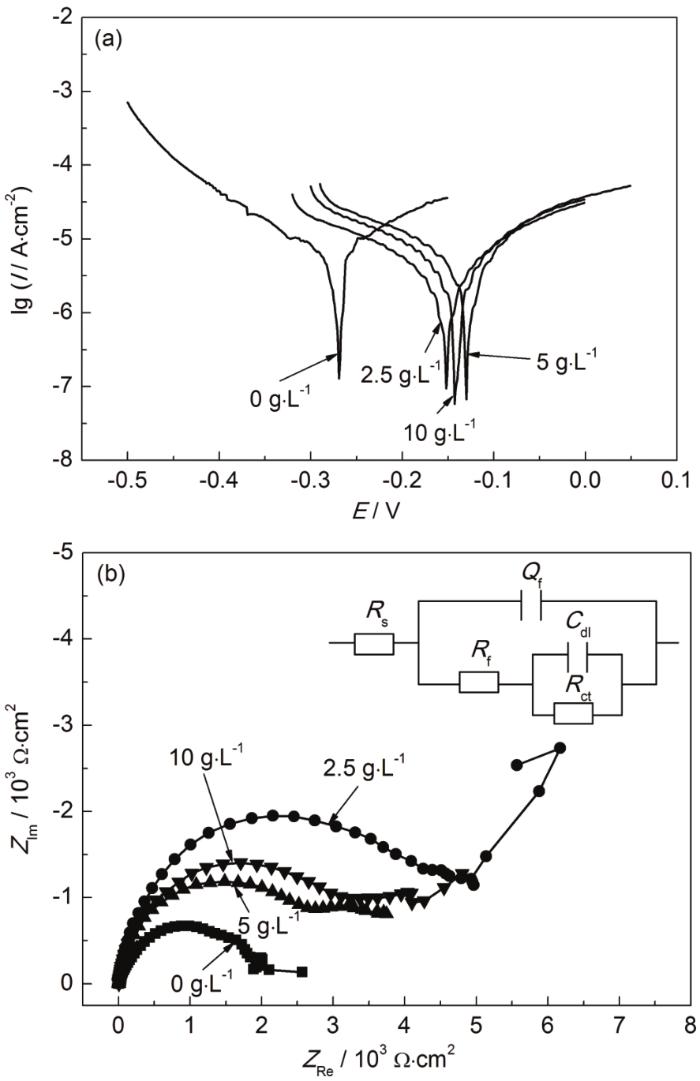
图8 不同K2C2O4浓度条件下Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的动电位极化曲线和电化学阻抗谱
表4 Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的极化曲线和EIS拟合参数

图8b为不同浓度K2C2O4镀液中所制备的Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的Nyquist图及选用的等效电路图。采用R(Q(R(CR))) 等效电路对结果进行拟合,EIS的拟合参数值列在表4中。可知,当K2C2O4浓度为2.5 g·L-1时所制备的镀层的Rf为4648 Ω·cm2,Rct为4420 Ω·cm2,其数值均较大,Rf和Rct的数值越大,表明其耐蚀性越好,这与采用极化曲线拟合的结果基本一致。
2.5 Ni-Cr-P三元合金镀层的微观组织和耐蚀性能
基于2.1~2.4节研究的结果,确定制备典型Ni-Cr-P三元镀层试样的镀液配方及施镀工艺如下:10 g·L-1 NiSO4,10 g·L-1 NaH2PO2,5 g·LL-1CrCl3,10 g·L-1 Na3C6H5O7,1 mg·L-1 CH4N2S,20 mL·L-1 C3H6O3,0.1 g·L-1 C2H5NO2,2.5 g·L-1 K2C2O4,5 g·L-1 CHKO2,镀液pH值为4.6,施镀温度85 ℃,施镀时间1 h。通过称重法测出镀层的沉积速率为5.21 μm·h-1,并与Ni-P二元镀层进行对比研究。
图9a为Ni-P二元镀层和Ni-Cr-P三元镀层在0.5 mol·L-1的硫酸溶液中的极化曲线,表5为图9的极化曲线和EIS的部分拟合参数。材料在同一介质中,通常自腐蚀电位越正,自腐蚀电流越小,该材料的耐腐蚀性能就越好。由图9a和表5可以看到,Ni-Cr-P三元镀层的自腐蚀电位明显高于Ni-P二元镀层的,提高了大约0.25 V;其自腐蚀电流密度降低了大约两个数量级,表明三元Ni-Cr-P镀层的耐蚀性明显优于Ni-P二元镀层的。
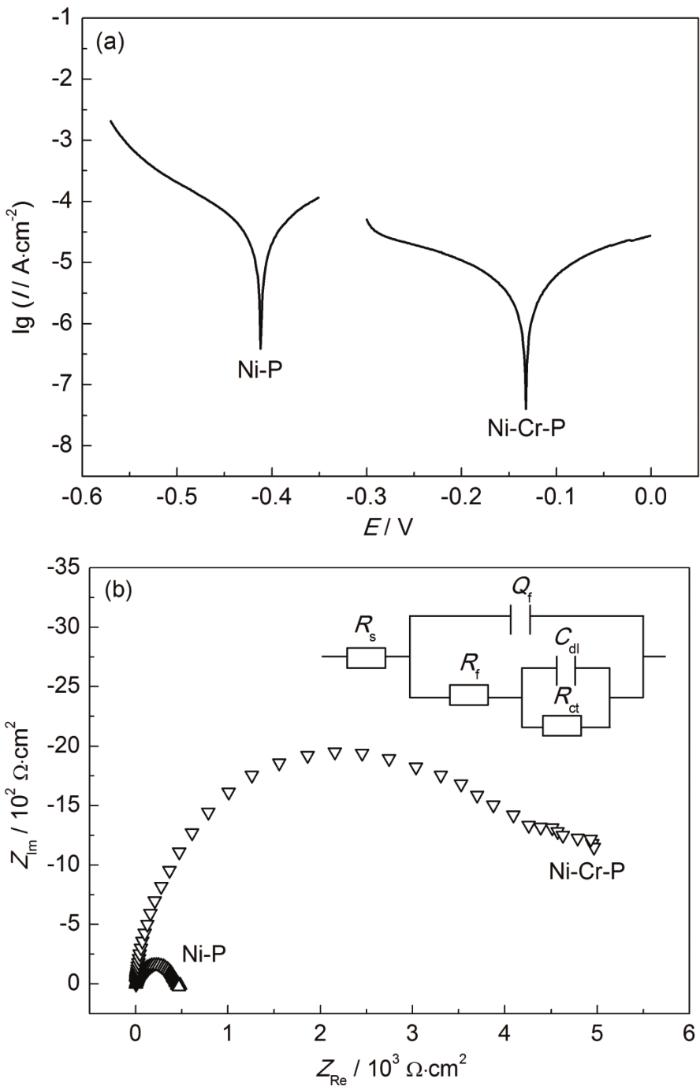
图9 Ni-P和Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的动电位极化曲线和电化学阻抗谱
表5 Ni-Cr-P镀层在0.5 mol·L-1硫酸溶液中的极化曲线和EIS拟合参数
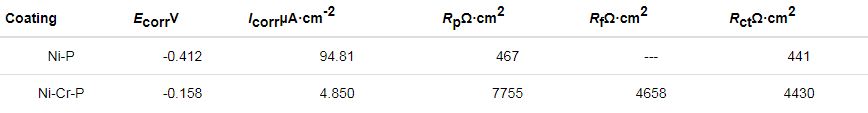
图9b为Ni-P二元镀层和Ni-Cr-P三元镀层在0.5 mol·L-1硫酸溶液中的Nyquist图及选用的等效电路图。采用R(Q(R(CR))) 等效电路图对结果进行拟合。EIS的拟合部分参数值列在表5中。Ni-Cr-P三元镀层的Rf为4658 Ω·cm2,Rct为4430 Ω·cm2,其数值相对Ni-P二元镀层均较大,表明Ni-Cr-P三元合金镀层耐蚀性比Ni-P二元镀层好,这个阻抗拟合结果和采用极化曲线拟合的结果一致。另外,由图9b的Nyquist图也可看出,Ni-Cr-P三元镀层的容抗弧半径更大。文献[24]指出,Nyquist图中容抗弧半径尺寸可表征涂镀层阻抗性能,半径越大,电子转移越难,涂镀层的电阻越大,耐腐蚀性越好,此结果从另一个方面验证了Ni-Cr-P三元镀层具有更好的抗腐蚀性能。
图10是化学镀Ni-Cr-P三元镀层的表面SEM像。可以看出,Ni-Cr-P三元镀层表面呈胞状结构,且颗粒分布较均匀,排列较致密,相应的镀层表面较为光滑。

图10 Ni-Cr-P合金镀层的表面形貌
图11为化学镀Ni-Cr-P三元镀层的XRD谱。可以看出,Ni-Cr-P镀层的XRD谱在2θ=45°附近形成下部较宽的“馒头”状峰,可知是Ni的 (111) 衍射方向有漫散射的衍射峰,表明此时镀层是非晶态加微晶态结构,这与文献[13]结果相近。此外,镀层中还存在少量Cr3Ni2相。有研究[16,17]指出,Ni-Cr-P三元镀层形成非晶所需的P含量低于Ni-P二元镀层的,Cr的存在有利于非晶结构的形成,Cr富集在镀层外表面,使镀层的自钝化倾向加强,耐蚀性提高。如何进一步提高镀层表面Cr含量还有待进一步研究。
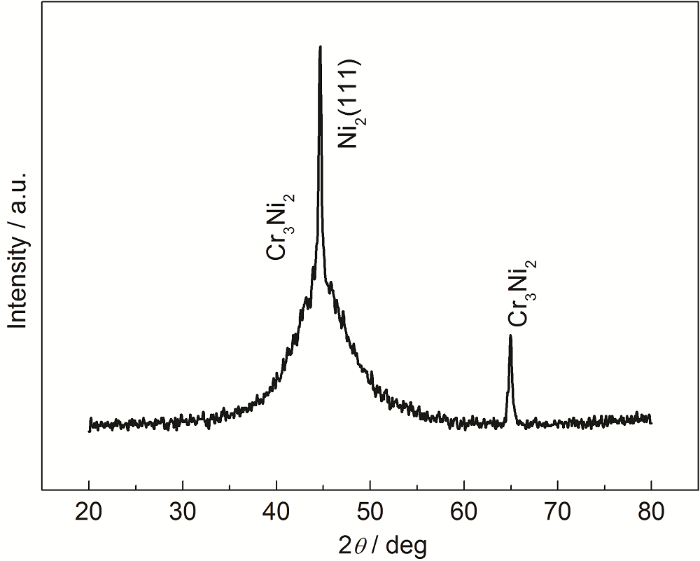
图11 Ni-Cr-P合金镀层的XRD谱
3 结论
(1) 随着镀液中的CrCl3浓度增加,沉积速率提高,镀液变得不稳定。C3H6O3,C2H5NO2,K2C2O4浓度增加,沉积速率降低,镀液稳定。化学镀法制备的Ni-Cr-P镀层表面形貌呈胞状结构,镀层为非晶和微晶混合结构。
(2) 在0.5 mol·L-1硫酸溶液中,Ni-Cr-P三元镀层的自腐蚀电位远高于Ni-P二元合金镀层的,向正移动约0.25 V;其电荷转移电阻增大,腐蚀电流密度降低了大约两个数量级,化学镀Ni-Cr-P三元镀层的耐蚀性明显优于Ni-P二元合金镀层的。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。
-
标签: 化学镀, Ni-Cr-P合金镀层, 配位剂, 电化学阻抗, 极化曲线

官方微信
《中国腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606-806
- 邮箱:fsfhzy666@163.com
- 中国腐蚀与防护网官方QQ群:140808414





