摘要
运用循环阳极极化曲线研究了不同温度和浓缩度的海水介质中316L不锈钢的点蚀行为. 结果表明, 在1~3倍浓缩度范围内, 316L不锈钢的点蚀电位和再钝化电位均随着温度的升高而线性降低, 但当浓缩度高于2倍、温度大于85 ℃时, 点蚀电位变化较小; 在25~95 ℃温度范围内, 点蚀电位和再钝化电位与海水浓缩度的对数呈线性关系. 浓缩度对316L不锈钢点蚀性能的影响比温度更小, 并根据点缺陷理论分析了二者对点蚀的作用机制.
关键词: 不锈钢 ; 点蚀 ; 浓缩海水 ; 温度
本文引用格式
辛森森, 李谋成, 沈嘉年. 海水温度和浓缩度对316L不锈钢点蚀性能的影响*[J]. , 2014, 50(3): 373-378 https://doi.org/10.3724/SP.J.1037.2013.00314
XIN Sensen, LI Moucheng, SHEN Jianian. EFFECT OF TEMPERATURE AND CONCENTRATION RATIO ON PITTING RESISTANCE OF 316L STAINLESS STEEL IN SEAWATER[J]. 金属学报, 2014, 50(3): 373-378 https://doi.org/10.3724/SP.J.1037.2013.00314
随着世界各国经济的高速发展以及人口的迅速增长和集中, 世界各国对水的需求日益增加, 而地球上的淡水资源非常有限, 淡水资源缺乏已成为全球性的问题. 为了解决水资源短缺这一难题, 人们把目光投向了取之不尽的海水, 海水淡化技术应运而生. 海水淡化是指脱除海水中的大部分盐分, 使其符合用水标准的水处理技术. 海水淡化技术的种类很多, 但适用于产业化的主要有反渗透法和蒸馏法[1-3]. 这2种方法都会使海水淡化设备处于腐蚀性较强的浓缩海水环境中, 对用材的耐蚀性要求较高. 低温多效蒸馏法等热法海水淡化设备常采用耐点蚀性能良好的奥氏体316L不锈钢进行制造. 然而, 为了进一步提高热量利用率和淡水出水率, 需调整海水淡化生产工艺, 提高海水的温度或者浓缩度[4,5]. 但这会使不锈钢海水淡化设备更容易遭受腐蚀, 尤其是高浓度Cl-的点蚀作用.
国内外学者研究了Cl-和温度对不锈钢点蚀的影响[6-19]. Frankel等[20]和 Hunkeler等[21]研究发现, 不锈钢的点蚀电位随着Cl-浓度的对数增加呈线性减小. Malik等[22]通过研究316L不锈钢在不同Cl-浓度溶液中点蚀行为, 发现随着Cl-浓度的增加, 点蚀的数量和深度不断增加. Park等[23]通过研究温度和Cl-浓度对304不锈钢点蚀萌生和早期点蚀生长的影响, 认为随着Cl-浓度增加和温度的升高, 点蚀更容易生长, 点蚀电位趋于减小, 尤其温度更利于促进点蚀的生长和抑制再钝化. 与文献报道不同的是, 浓缩海水组分多且含量高. 本工作运用循环阳极极化曲线研究316L不锈钢在25~95 ℃温度范围内、1~3倍浓缩海水中的点蚀规律与机制, 为低温多效蒸馏法等热法海水淡化设备的选材与运行工艺控制提供依据.
1 实验方法
电极材料采用316L不锈钢, 其主要化学成分(质量分数, %)为: C 0.023, P 0.034, S 0.004, Si 0.57, Mn 1.37, Mo 2.05, Cr 16.4, Ni 10.3, Cu 0.14, N 0.039, Fe余量. 每个试样电极背面焊接导线, 然后用环氧树脂封装, 露出1 cm2工作面积. 在使用之前, 工作电极用SiC砂纸依次打磨至1000号, 并用去离子水和酒精清洗表面.
实验溶液由分析纯试剂和去离子水配置而成. 按照ASTM D1141标准人工海水成分(NaCl, MgCl2, Na2SO4, CaCl2, KCl, NaHCO3, KBr和SrCl2的浓度分别为24.53, 5.20, 4.09, 1.16, 0.70, 0.20, 0.10和0.03 g/L), 分别配制浓缩度CR为1, 1.5, 2, 2.5和3倍的海水. 溶液pH值用0.1 mol/L的NaOH溶液调至8.2. 实验溶液温度分别为25, 50, 63, 72, 85和95 ℃. 其中, 1.5倍浓缩度和63~72 ℃为低温多效蒸馏法海水淡化技术常用工艺参数.
电化学测量均在三电极电解池中进行, 以饱和甘汞为参比电极(SCE), Pt电极为辅助电极. 实验过程中用恒温水浴锅控制电解池温度. 电化学测试系统由PAR 273A恒电位仪及Powersuite软件组成. 循环阳极极化曲线测试方法为: 测试前试样在溶液中浸泡1 h以获得相对稳定的腐蚀电位, 然后以20 mV/min的速率进行正向扫描, 当电流密度达到1 mA/cm2时改变电位扫描方向, 获得循环极化曲线. 为了保证实验结果的可重现性, 在每个温度每个海水浓缩度下, 测试3个平行试样. 极化曲线测量后用JSM-6700F高分辨扫描电镜(SEM)对试样表面进行观察.
2 实验结果与分析
2.1温度对点蚀性能的影响
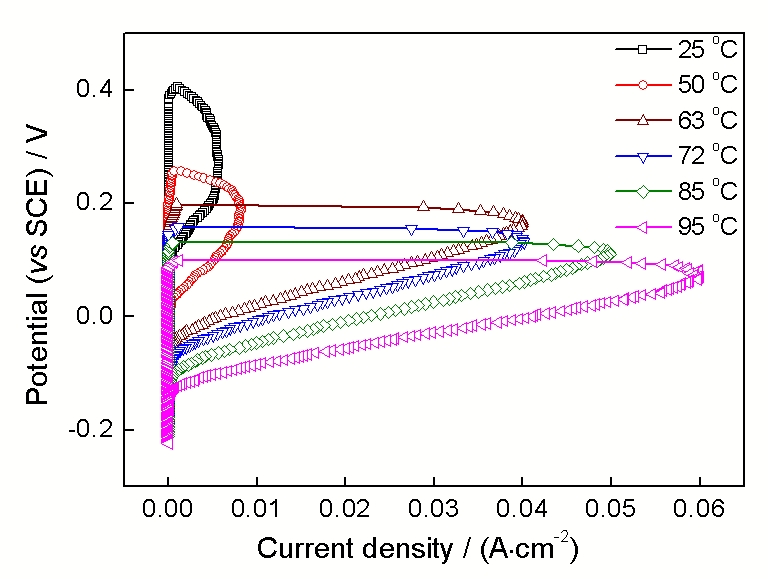
实验测试了316L不锈钢在不同温度和不同浓缩度海水环境中的循环阳极极化曲线, 由于各条件下的曲线形状相似, 仅给出了1.5倍浓缩海水中各温度下的典型曲线, 如图1所示. 可以看出, 在所有温度下, 316L不锈钢均具有良好钝化状态; 当电位升高到某一临界值时, 曲线出现拐点, 电流密度突然快速增加, 这时不锈钢表面钝化膜发生破坏, 出现点蚀现象. 很明显, 随着海水温度升高, 发生点蚀的电位和再钝化电位均不断下降. 点蚀电位EP和再钝化电位ER均相差几百毫伏. 浓缩度为1~3倍的海水环境中, EP和ER均随着溶液温度的升高而明显降低, 表明溶液温度对316L不锈钢的耐腐蚀性具有较大影响.
Fig.1 不同温度下在浓缩度为1.5倍的海水中316L不锈钢的循环阳极极化曲线
不同温度下阳极极化测量后, 316L不锈钢电极表面的点蚀形貌具有类似形状, 图2给出了72 ℃下浓缩度为1.5倍的海水中电极极化后典型点蚀形貌的SEM像. 蚀坑均具有多孔的花边盖状特征; 随着溶液温度的升高, 蚀坑的尺寸略有增大. 可见, 316L不锈钢极化后形成了闭塞点蚀坑, 温度升高对其生长有一定加速作用.
Fig.2 316L不锈钢在1.5倍浓缩海水中72 oC下阳极极化后的点蚀形貌
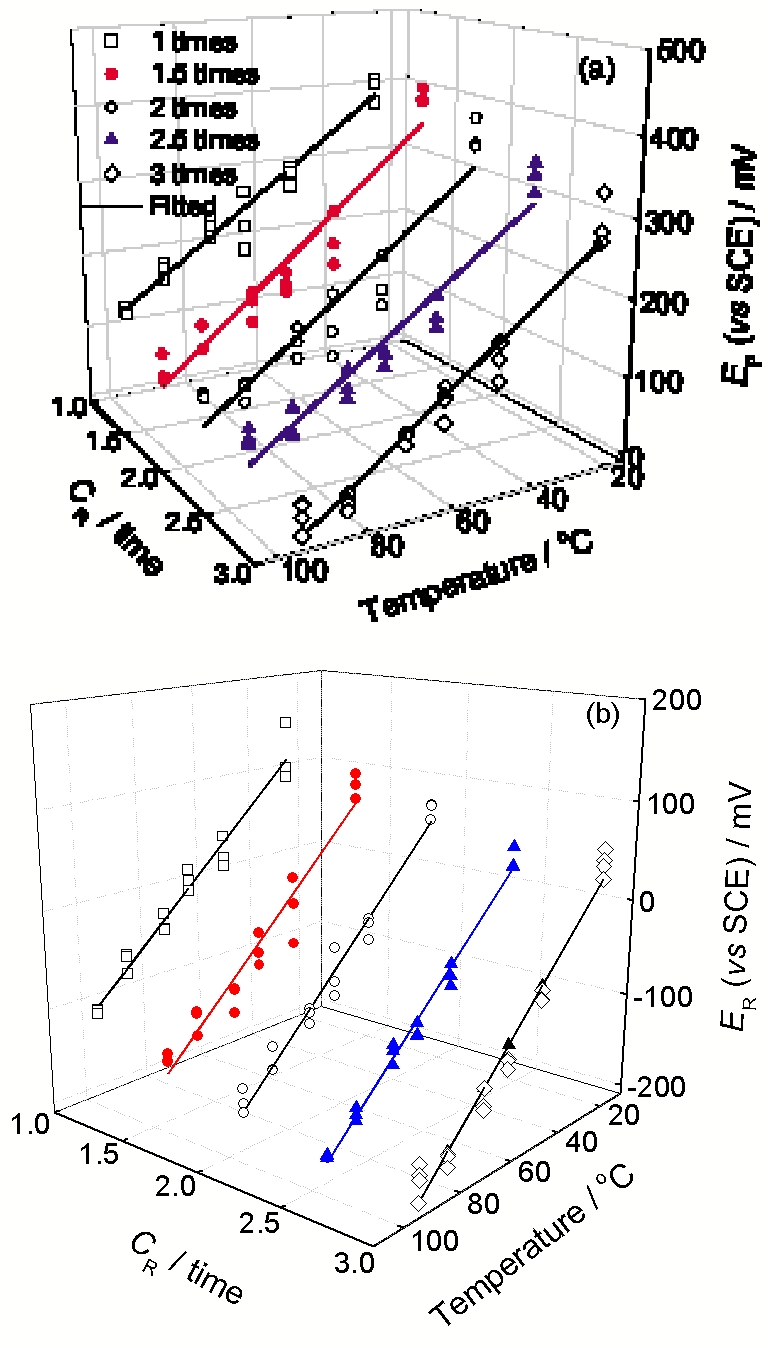
从循环阳极极化曲线中可以分别获得不同浓缩度和温度下的EP与ER, 进而分析海水浓缩度和温度对316L不锈钢点蚀性能的作用规律. 图3给出了不同海水浓缩度下温度与EP和ER的关系曲线. 可见, 不同海水浓缩度下, 点蚀电位和再钝化电位均随着溶液温度升高而呈线性降低, 但当浓缩度高于2倍、温度大于85 ℃时, 点蚀电位变化较小, 偏离线性关系. 这些变化规律与不同NaCl浓度条件下获得的规律[8,24]相同. 该线性关系可表达为:

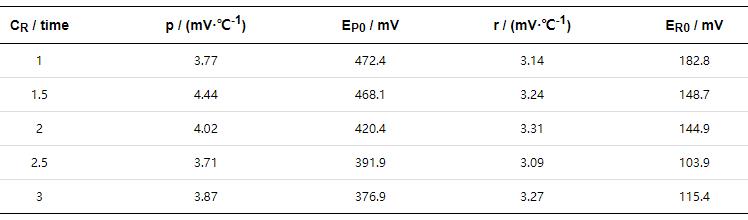
式中, T为热力学温度, p和r为斜率常数, EP0和ER0为截距常数. 表1列出了图1中不同浓缩度的线性拟合结果. 浓缩度从1倍增大到3倍时, p值范围在3.71~4.44 mV/℃, 变化区间非常小; r值变化范围为3.09~3.31 mV/℃, 变化区间也比较小, 表明浓缩度对点蚀机制的作用较小. 由此可知, 不同浓缩度下316L具有相似的点蚀机制, 但耐点蚀性能及其再钝化能力均随着温度升高而呈现线性减小趋势.
Fig.3 不同浓缩度下316L不锈钢的点蚀电位EP和再钝化电位ER与溶液温度的关系曲线
根据点缺陷模型(PDM)[25,26], 材料表面存在着大量缺陷, 活性阴离子Cl-优先吸附在缺陷部位形成吸附物, 随着Cl-吸附物的不断增多, 钝化膜的稳定性逐渐降低, 最终导致钝化膜破坏而发生点蚀. 随着浓缩海水温度的升高, 溶液的对流和扩散增强, Cl-扩散速度也会增大, 更加容易扩散进入钝化膜, 并在不锈钢表面缺陷处形成更多Cl-吸附物, 这时钝化膜的局部溶解过程会被加快, 从而导致钝化膜的致密性降低而加速破坏. 另一方面, 随着温度升高, 浓缩海水中的溶解氧含量逐渐减少, 会导致钝化膜的形成过程受到限制. 因此, 随着浓缩海水温度的升高, 316L不锈钢的点蚀电位和再钝化电位不断降低, 耐点蚀性能线性下降.
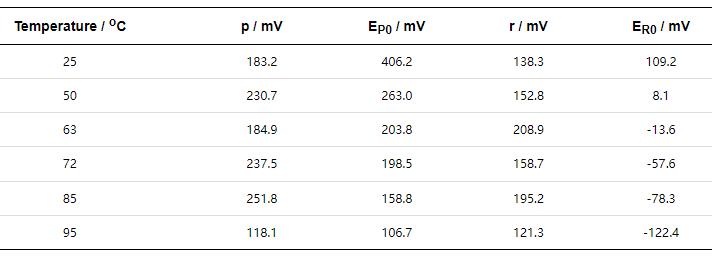
表1 点蚀电位和再钝化电位与温度间的线性拟合结果
2.2 浓缩度对点蚀性能的影响
图4给出了316L不锈钢在72 ℃下不同浓缩度海水中的典型循环阳极极化曲线. 可以看出, 316L不锈钢在不同浓缩度的海水中均具有钝化状态. EP和ER均随着海水浓缩度的增大而降低, 海水浓缩度对316L不锈钢的耐腐蚀性也具有明显影响.
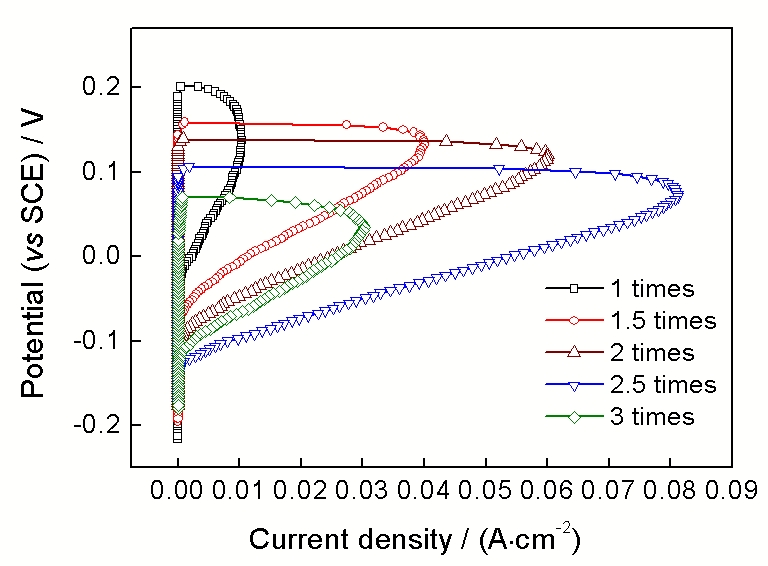
Fig.4 316L不锈钢在72 ℃下不同浓缩度海水中的循环阳极极化曲线
图5给出了不同温度下EP和ER随海水浓缩度的变化曲线. 可以看出, EP和ER随海水浓缩度的增加而减小, 其值均与海水浓缩度的对数呈线性变化规律, 可表示为:

表2列出了图5中不同温度下各参数的拟合结果. 可见, 溶液温度由25 ℃升高到95 ℃时, p值变化范围为118.1~251.8 mV, r值范围为121.3~208.9 mV, 变化区间均较小, 表面浓缩度的变化未改变316L的点蚀机制. EP0和ER0均随温度升高而呈现减小趋势, 变化幅度分别可达300 和230 mV. 因此, 不同温度下316L具有相似的点蚀机制, 但耐点蚀性能及其再钝化能力均随着浓缩度增大而呈现半对数下降趋势.
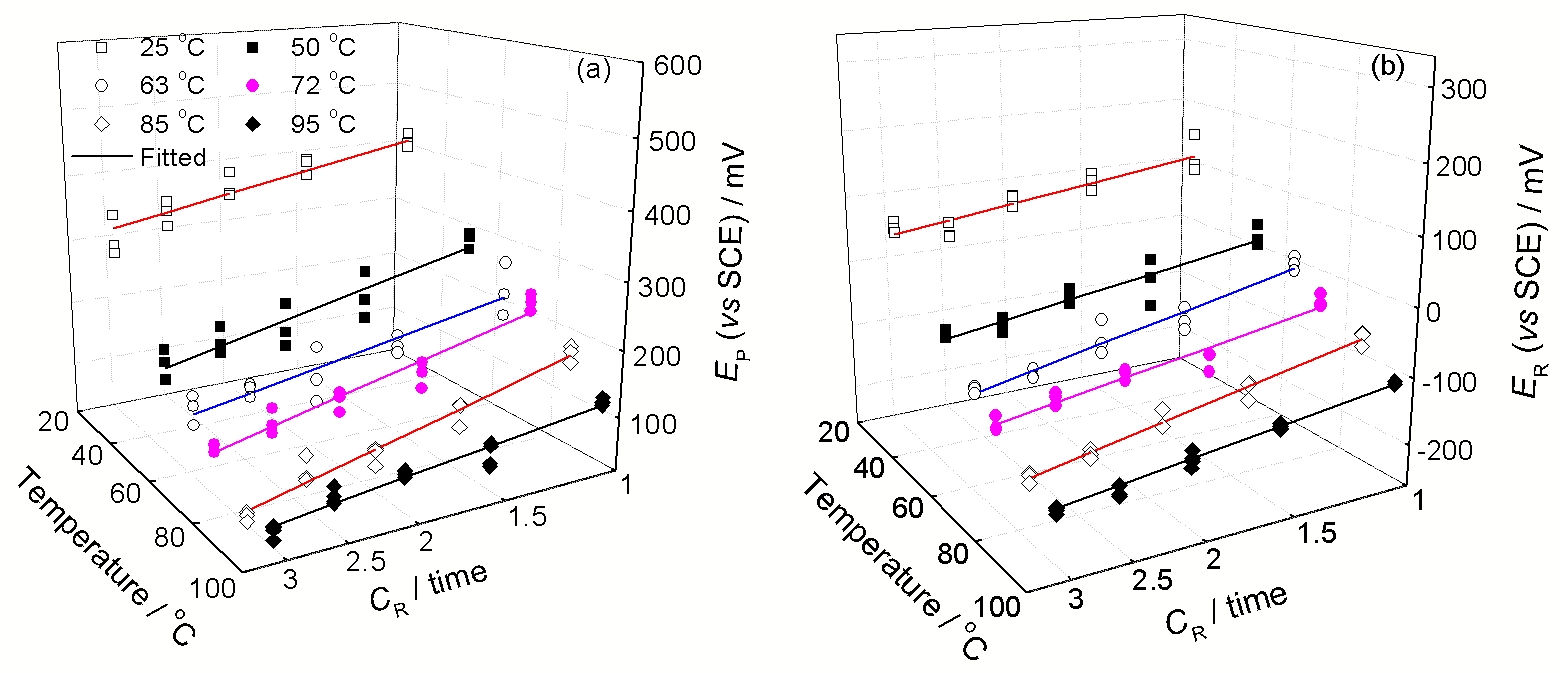
Fig.5 不同温度下316L不锈钢的Ep和ER与海水浓缩度的关系曲线
文献[24]和[26]中报道, SO42-对Cl-引起的点蚀具有抑制作用, 但是, 本实验条件下不同浓缩度海水环境中的[SO42-] / [Cl-]比值是1∶19.2, 相对于Cl-对点蚀的影响而言, SO42-含量极少, 根据竞争吸附理论, SO42-对点蚀性能的影响很小, 316L不锈钢的点蚀行为决定于浓缩海水中Cl-的作用. Cl-通过吸附并进入钝化膜, 从而导致点蚀诱发. 根据PDM模型[25,26], 引入阳离子空位、O空位和金属阳离子间隙作为钝化膜中的缺陷, 钝化膜的生长、溶解和破坏是由这些缺陷的生成和消失决定的. 在浓缩海水中, Cl-含量高, 很容易被吸附进入O空位, 从而促使反应形成大量的阳离子空位. 当阳离子空位聚积到一定的临界尺寸时, 将在金属/钝化膜界面形成空洞, 引起局部钝化膜的破裂. 溶液中Cl-含量随浓缩度增大而升高, 无疑会增强这种缺陷反应, 因此, 随着海水浓缩度增大, 316L不锈钢的点蚀电位和再钝化电位不断降低(图5), 耐点蚀性能与其对数间呈线性下降规律.
2.3 温度和浓缩度对点蚀性能的相对作用程度
从表1和2可知, p和r均未随温度和浓缩度呈现规律性变化趋势, 不能用以对比分析温度和浓缩度对点蚀性能的影响程度. 然而, 对现行的低温多效蒸馏法海水淡化工艺条件而言, 最高运行温度为72 ℃, 海水浓缩度不高于1.5倍, 如果不改变浓缩度, 将温度升高10%, 变为79.2 ℃, 利用式(1)和(2)计算可知, 点蚀电位和再钝化电位将分别从148.4和-85.1 mV 下降到116.5和-108.4 mV, 降低幅度分别为31.9和23.3 mV; 如果不改变温度, 将浓缩度增大10%变为1.65倍浓缩度, 利用式(3)和(4)计算可知, 点蚀电位和再钝化电位将分别从156.7和-85.5 mV下降到146.8 和-92 mV, 降低幅度分别为9.9和6.5 mV. 此外, 从点蚀电位来看, 浓缩度增大36%到2.04倍, 才可能像温度升高10%那样导致点蚀电位降低31.9 mV. 显然, 海水浓缩度对316L不锈钢点蚀性能的影响比温度更小. 由此可推知, 相对于温度变化, 热法海水淡化工艺中海水浓缩度变化对不锈钢设备腐蚀性能的影响更小, 提高海水浓缩度对不锈钢设备使用寿命的影响较小.
表2 点蚀电位和再钝化电位与海水浓缩度对数间线性拟合结果
3 结论
(1) 在不同浓缩度的海水中, 316L不锈钢的点蚀电位和再钝化电位均随着温度升高而线性下降, 但当浓缩度高于2倍、温度大于85 ℃时, 点蚀电位变化较小, 偏离线性关系; 在不同温度的浓缩海水中, 316L不锈钢的点蚀电位和再钝化电位均随着海水浓缩度的增加而减小, 与海水浓缩度的对数呈线性关系. 温度和浓缩度的增加均会导致316L不锈钢的耐腐蚀性能降低, 可运用PDM模型解释其作用机制.
(2) 浓缩海水环境中, 温度和浓缩度对316L不锈钢点蚀性能的影响程度有差异, 温度对点蚀性能的影响更大. 在低温多效蒸馏法等热法海水淡化工艺中, 与温度相比, 海水浓缩度的调整或波动对316L不锈钢设备腐蚀性能的影响相对较小.
参考文献
[1] Wade N W. Desalination, 1993; 93: 343
[2] Olsson J. Desalination, 2005; 183: 217
[3] Khawaji A D, Kutubkhanah I K, Wie J M. Desalination, 2008; 221: 47
[4] Budhiraja P, Fares A A. Desalination, 2008; 220: 313
[5] Al-Shammiri M, Safar M. Desalination, 1999; 126: 45
[6] Hospadaruk V, Petrocelli J V. J Electrochem Soc, 1966; 113: 878
[7] Moayed M H, Laycock N J, Newman R C. Corros Sci, 2003; 45:1203
[8] Laycock N J, Newman R C. Corros Sci, 1988; 40: 887
[9] Hong T, Nagumo M. Corros Sci, 1997; 39: 288
[10] Moretti G, Quartarone G, Tassan A, Zingales A. Mater Corros, 1993; 44: 24
[11] Tsutsumi Y, Nishikata A, Tsuru T. Corros Sci, 2007; 49: 1394
[12] Cheng X Q, Li X G, Du C W. Acta Metall Sin, 2006; 42: 299
[12] (程学群, 李晓刚, 杜翠薇. 金属学报, 2006; 42: 299)
[13] Liao J X, Jiang Y M, Wu W W, Zhong C, Li J. Acta Metall Sin, 2006; 42: 1187
[13] (廖家兴, 蒋益明, 吴玮巍, 钟 澄, 李 劲. 金属学报, 2006; 42: 1187)
[14] Yashiro H, Tanno K, Koshiyama S, Akashi K. Corrosion, 1996; 52: 109
[15] Sikora J, Sikora E, Macdonald D D. Electrochim Acta, 2000; 45: 1875
[16] Wang J H, Su C C, Szklarska-Smialowska Z. Corrosion, 1988; 44: 732
[17] Stockert L, Hunkeler F, Bohni H. Corrosion, 1985; 41: 676
[18] Wei X, Dong J H, Tong J, Zheng Z, Ke W. Acta Metall Sin, 2012; 48: 502
[18] (魏 欣, 董俊华, 佟 健, 郑 志, 柯 伟. 金属学报, 2012; 48: 502)
[19] Li M C, Zeng C L, Lin H C, Cao C N. Acta Metall Sin, 2002; 36: 1287
[19] (李谋成, 曾潮流, 林海潮, 曹楚南. 金属学报, 2002; 36: 1287)
[20] Frankel G S, Stockert L, Hunkeler F, Bohni H. Corrosion, 1987; 43: 429
[21] Hunkeler F, Frankel G S, Bohni H. Corrosion, 1987; 43: 189
[22] Malik A U, Mayan Kutty P C, Siddiqi N A, Andijani I N, Ahmed S. Corros Sci, 1992; 33: 1809
[23] Park J O, Matsch S, Bohni H. J Electrochem Soc, 2002; 149: 34
[24] Leckie H P, Uhlig H H. J Electrochem Soc, 1966; 115: 1262
[25] Macdonald D D. J Electrochem Soc, 1992; 139: 3434
[26] Macdonald D D. Electochim Acta, 2011; 56: 1761
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808414